题目内容
5.下列物质中含有非极性键的共价化合物是( )| A. | H2O2 | B. | CH4 | C. | Na2O2 | D. | I2 |
分析 化合物中至少含有两种元素,共价化合物中不含离子键,同种非金属元素之间以非极性键结合,以此来解答.
解答 解:A.过氧化氢中含有O-O非极性键,O-H极性键,则为含有非极性键的共价化合物,故A正确;
B.CH4中只含有极性共价键,为含有极性键的共价化合物,故B错误;
C.Na2O2中含有离子键和非极性键,则为含有非极性键的离子化合物,故C错误;
D.I2中只含有非极性键,是单质不是化合物,故D错误.
故选A.
点评 本题考查极性键和非极性键,熟悉常见元素之间的成键是解答本题的关键,并注意离子化合物与共价化合物的区别来解答,题目难度不大.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
16.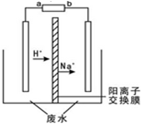 2016年两会3月2日在北京拉开帷幕,在涉及国计民生的众多提案中,“水资源的保护和合理利用”仍然是人民群众关注的焦点.最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸,总反应如下:2CH3CHO+H2O$\frac{\underline{\;电解\;}}{\;}$CH3CH2OH+CH3COOH实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示.下列有关说法不合理的是( )
2016年两会3月2日在北京拉开帷幕,在涉及国计民生的众多提案中,“水资源的保护和合理利用”仍然是人民群众关注的焦点.最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸,总反应如下:2CH3CHO+H2O$\frac{\underline{\;电解\;}}{\;}$CH3CH2OH+CH3COOH实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示.下列有关说法不合理的是( )
 2016年两会3月2日在北京拉开帷幕,在涉及国计民生的众多提案中,“水资源的保护和合理利用”仍然是人民群众关注的焦点.最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸,总反应如下:2CH3CHO+H2O$\frac{\underline{\;电解\;}}{\;}$CH3CH2OH+CH3COOH实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示.下列有关说法不合理的是( )
2016年两会3月2日在北京拉开帷幕,在涉及国计民生的众多提案中,“水资源的保护和合理利用”仍然是人民群众关注的焦点.最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸,总反应如下:2CH3CHO+H2O$\frac{\underline{\;电解\;}}{\;}$CH3CH2OH+CH3COOH实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示.下列有关说法不合理的是( )| A. | 若以锌-锰碱性电池为直流电源,则b极材料为Zn | |
| B. | 已知乙醛、乙醇的沸点分别为20.8℃、78.4℃,从电解后的溶液中分离出乙醇粗产品的方法是蒸馏 | |
| C. | 若反应过程中每生成1mol乙醇,理论上至少消耗氢气11.2L | |
| D. | 电解过程中,阳极除生成氧气外,还发生如下反应:CH3CHO+2H2O-2e-=CH3COOH+2H+ |
13.下列化学性质中,烷烃不具备的是( )
| A. | 一定条件下发生分解反应 | B. | 可以在空气中燃烧 | ||
| C. | 光照条件下与Cl2发生取代反应 | D. | 能使酸性高锰酸钾溶液褪色 |
20.可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是( )
| A. | 将混合气体通过盛有KMnO4酸性溶液的洗气瓶 | |
| B. | 将混合气体通过盛有适量溴水的洗气瓶 | |
| C. | 将混合气体通过盛有水的洗气瓶 | |
| D. | 将混合气体通过盛有澄清石灰水的洗气瓶 |
10.2008年北京奥运会火炬使用丙烷作燃料丙烷属于( )
| A. | 无机物 | B. | 烷烃 | C. | 氧化物 | D. | 可燃性单质 |
17.下列对物质用途的描述中,错误的是( )
| A. | 浓硫酸可用于干燥NH3、H2、O2等气体 | |
| B. | 二氧化硫可用来漂白纸浆、毛、丝等 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 干冰升华没有断裂化学键 |
14.有A、B、C、D四块金属,若A、B用导线相连成原电池时,A为负极;若C、D相连构成原电池时,电流由D流向C;A、C相连浸入稀硫酸中时,C极上产生大量气泡;把D投入到B的硫酸盐溶液中,D的表面有B析出;则四种金属的活动性顺序为( )
| A. | B>D>C>A | B. | C>A>B>D | C. | A>C>D>B | D. | A>B>C>D |
15.下列有关说法正确的是( )
| A. | 1mol Fe与足量的非金属反应转移电子为2mol | |
| B. | 1mol Fe与足量的硝酸反应转移电子为3mol | |
| C. | 1mol FeCl3与足量Zn反应转移电子为2mol | |
| D. | 1mol FeCl2与足量Cu反应转移电子为2mol |
 如图是用来电解CuCl2溶液的装置图,在U形管中注入CuCl2溶液,插入A.B两根石墨棒作电极.回答下列问题:
如图是用来电解CuCl2溶液的装置图,在U形管中注入CuCl2溶液,插入A.B两根石墨棒作电极.回答下列问题: