题目内容
【题目】氮化铝(AlN)是一种新型无机非金属材料。某AlN样品仅含有Al2O3杂质,为测定AlN的含量,设计如下两种实验方案。已知:AlN+NaOH+H2O═NaAlO2+NH3↑
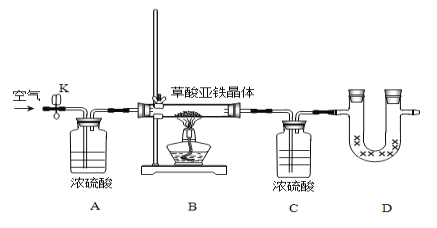
(方案 1)取一定量mg 的样品,用图1装置测定样品中AlN的纯度(夹持装置已略去)。
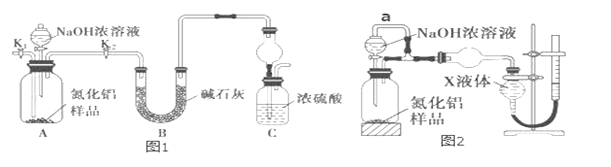
(1)如图 1,C 装置中球形干燥管的作用是_____。
(2)完成以下实验步骤:组装好实验装置,首先检查装置气密性,再加入实验药品。接下来的实验操作是______________ ,打开分液漏斗活塞,加入 NaOH 浓溶液,至不再产生气体。打开 K1,通入氮气一段时间,测定 C 装置反应前后的质量变化。通入氮气的目的是___________。
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见_____。
(方案 2)用图 2 装置测定 mg 样品中 AlN 的纯度(部分夹持装置已略去)。
(4)为测定生成气体的体积,量气装置中的X液体可以是_____。(填字母序号)
a.CCl4 b.H2O c.NH4Cl 溶液 d.C6H6(苯)
(5)若 mg 样品完全反应,测得生成气体的体积为 VmL(已转换为标准状况),则 AlN 的质量分数是_____________。
【答案】防止倒吸关闭 K1,打开 K2把装置中残留的氨气全部赶入 C 装置C 装置出口处连接一个干燥装置ad![]() ×100%
×100%
【解析】
在图1中,AlN和NaOH溶液反应生成氨气,经碱石灰干燥后被浓硫酸吸收,准确测定C装置增重的质量计算AlN的含量;在图2中,AlN和NaOH溶液反应生成氨气,利用排液体法测定氨气的体积计算AlN的含量。
(1).在装置A中,AlN和NaOH溶液反应生成氨气,氨气与浓硫酸发生反应,易发生倒吸,C装置中球形干燥管的作用是防止倒吸,故答案为:防止倒吸;
(2).组装好实验装置,先检查装置气密性,加入实验药品。接下来的实验操作是关闭K1,打开K2,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是把装置中残留的氨气全部赶入装置C被浓硫酸吸收,故答案为:关闭 K1,打开 K2;把装置中残留的氨气全部赶入C装置;
(3).装置存在的缺陷是空气中的水蒸气也可以进入装置C,使测定结果偏高,改进的措施是在C装置出口处连接一个干燥装置,故答案为:C装置出口处连接一个干燥装置;
(4).a.CCl4不能溶解氨气,可以用排四氯化碳溶液的方法测定氨气体积,故a正确;
b.氨气极易溶于水,不能用排水法测定,故b错误;
c.氨气极易溶于水,不能用排NH4Cl溶液的方法测定气体体积,故c错误;
d.氨气不溶于苯,可以利用排苯溶液的方法测定氨气的体积,故d正确,答案选:ad;
(5).若mg样品完全反应,测得生成气体的体积为VmL(已转换为标准状况),
AlN+NaOH+H2O═NaAlO2+NH3↑
41 22.4L
m V×103L
m=![]() g,则AlN的质量分数为
g,则AlN的质量分数为![]() ×100%=
×100%=![]() ×100%,故答案为:
×100%,故答案为:![]() ×100%。
×100%。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
a | b | c | |||||||||||||||
e | f | ||||||||||||||||
试回答下列问题:
(1)写出元素e的基态原子电子排布式________________,其未成对电子数为________。
(2)c在空气中燃烧产物的分子构型为_____,中心原子的杂化形式为______杂化。c能形成一种八元环状形同王冠的单质分子,原子的杂化形式为______杂化。
(3)b单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。
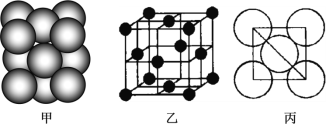
若已知b的原子半径为d厘米,NA代表阿伏加德罗常数,b的相对原子质量为M,请回答:
①晶胞中b原子的配位数为_____,表示原子空间占有率的代数式为_____________。
②该晶体的密度为_____________g/cm3(用含有关字母的代数式表示)。a、f中,与单质b晶体中原子的堆积方式相同的是__________(填元素符号)。