题目内容
【题目】(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况.试判断,违反了泡利原理的是_____,违反了洪特规则的是______。
![]()
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为________;其最高价氧化物对应水化物的化学式是________。
(3)用符号“>”“<”或“=”表示下列各项关系。
①第一电离能:Na________Mg,Mg________Ca。
②电负性:O________F,F________Cl。
③能量高低:ns________(n+1)s,ns________np。
【答案】 ② ③ 1s22s22p63s23p4 H2SO4 < > < > < <
【解析】(1)泡利不相容原理:每个原子轨道上最多只能容纳2个自旋状态相反的电子;洪特规则:在同一个电子亚层中排布的电子,总是尽先占据不同的轨道,且自旋方向相同;
(2)同一元素的原子中,基态和激发态原子的核外电子总数相等,根据构造原理书写其基态原子核外电子排布式;在主族元素中,元素的最高化合价等于其族序数,从而确定其最高价氧化物对应的水化物;
(3)根据电负性、电离能的变化规律解答;电子的能层越大其能量越高,同一能层的电子,按s、p、d能量逐渐增大。
(1)泡利不相容原理:每个原子轨道上最多只能容纳2个自旋状态相反的电子,所以违反泡利不相容原理的是②;洪特规则是指在同一个电子亚层中排布的电子,总是尽先占据不同的轨道,且自旋方向相同,因此违反洪特规则的有③;
(2)根据激发态原子核外电子排布式知该元素核外有16个电子,根据构造原理知,其基态原子核外电子排布式为:1s22s22p63s23p4,该元素是S元素,S元素最外层有6个电子,其最高化合价是+6价,其最高价氧化物对应的水化物是硫酸,其化学式为H2SO4;
(3)①同一周期中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族元素大于相邻元素,同一主族元素中,元素的第一电离能随着原子序数的增大而减小,所以第一电离能:Na<Mg,Mg>Ca;
②同一周期中,元素的电负性随着原子序数的增大而增大,同一主族中,元素的电负性随着原子序数的增大而减小,所以电负性:O<F,F>Cl;
③电子的能层越大其能量越高,同一能层的电子,按s、p、d能量逐渐增大,所以能量高低:ns<(n+1)s,ns<np。

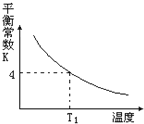
【题目】T2℃时,将1 mol X和2 mol Y投入2L的密闭容器中,发生反应:X(g)+2Y(g)![]() 3Z(g)ΔH,测得X、Y的量随时间变化如下表,平衡时物质X的体积分数为φ,该反应的平衡常数(K)随温度的变化如下图,则下列判断正确的是
3Z(g)ΔH,测得X、Y的量随时间变化如下表,平衡时物质X的体积分数为φ,该反应的平衡常数(K)随温度的变化如下图,则下列判断正确的是
0 | 1 | 2 | 3 | 4 | 5 | 6 | |
X | 1 | 0.80 | 0.66 | 0.58 | 0.52 | 0.50 | 0.50 |
Y | 2 | 1.60 |
A. 前5 min用Z表示的平均反应速率为1.2mol/(L·min)
B. T2℃时,对于反应1/2X(g)+Y(g)![]() 3/2Z(g) △H’ 2ΔH’=ΔH
3/2Z(g) △H’ 2ΔH’=ΔH
C. T2℃时,若以1mol X、2mol Y和1mol Z充入上述容器中,达到平衡时X的体积分数比φ大
D. 该反应的正反应是吸热反应,且T1<T2