题目内容
19.下列过程中,没有明显实验现象的是( )| A. | 加热溶有SO2的品红溶液 | |
| B. | 将HCl通入NaAlO2溶液中 | |
| C. | 向Fe(NO3)2溶液中滴加稀硫酸 | |
| D. | 向碳酸氢钠溶液中滴加氢氧化钠溶液 |
分析 A.二氧化硫能使品红溶液褪色,但二氧化硫的漂白性不稳定,受热易恢复原色;
B.HCl通入偏铝酸钠溶液中先生成氢氧化铝沉淀,当HCl过量时,沉淀会溶解;
C.酸性条件下,亚铁离子能被硝酸根离子氧化;
D.碳酸氢钠、NaOH、碳酸钠溶液都呈无色.
解答 解:A.二氧化硫能使品红溶液褪色,但二氧化硫的漂白性不稳定,受热易恢复原色,所以加热溶有SO2的品红溶液,溶液由无色变为红色,故A不选;
B.HCl通入偏铝酸钠溶液中先生成氢氧化铝沉淀,当HCl过量时,沉淀会溶解,所以看到的现象是:先生成沉淀后沉淀溶解,有明显现象,故B不选;
C.酸性条件下,亚铁离子能被硝酸根离子氧化生成铁离子,同时生成NO,溶液由浅绿色变为黄色,有明显现象,故C不选;
D.碳酸氢钠、NaOH、碳酸钠溶液都呈无色,碳酸氢钠和NaOH反应生成碳酸钠,反应前后溶液都呈无色,没有明显现象,故D选;
故选D.
点评 本题考查元素化合物性质,涉及二氧化硫漂白性、氢氧化铝两性、亚铁离子的还原性等知识点,为高频考点,易错选项是C,中性条件下硝酸根离子没有氧化性,为易错点.

练习册系列答案
相关题目
10.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答下列问题:
(1)常温下,某氨水的pH=12,则水电离的c(OH-)=1×10-12mol/L.若向该氨水中加入等体积、等物质的量浓度的盐酸,此时溶液中水电离的程度大于(填“大于”、“等于”或“小于”)氨水中水的电离程度.
(2)合成氨反应N2(g)+3H2(g)?2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡向左移动(填“向正反应方向”、“向逆反应方向”或“不”).
(3)一定温度下,在密闭容器中可发生下列反应:2N2O5(g)?4NO2(g)+O2(g).下表为反应在T1温度下的部分实验数据:则500s内N2O5的分解速率v(N2O5)=3×10-3mol•L-1•s-1;降温至T2,反应迸行l000s时测得c(NO2)=4.98mol•L-1,则反应2N2O5(g)?4NO2(g)+O2(g)的△H<0.(填“>”、“=“或“<“).
(4)最近美国Simons等科学家发明了使NH3直接用于燃料电池的方法,其装置用铂黑作电极、加入电解质溶液中,一个电极通人空气,另一电极通入NH3.其电池反应式为:4NH3+3O2=2N2+6H2O.你认为电解质溶液应显碱性(填“酸性”、“中性”或“碱性”),写出正极的电极反应方程式O2+2H2O+4e-=4OH-.
(1)常温下,某氨水的pH=12,则水电离的c(OH-)=1×10-12mol/L.若向该氨水中加入等体积、等物质的量浓度的盐酸,此时溶液中水电离的程度大于(填“大于”、“等于”或“小于”)氨水中水的电离程度.
(2)合成氨反应N2(g)+3H2(g)?2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡向左移动(填“向正反应方向”、“向逆反应方向”或“不”).
(3)一定温度下,在密闭容器中可发生下列反应:2N2O5(g)?4NO2(g)+O2(g).下表为反应在T1温度下的部分实验数据:则500s内N2O5的分解速率v(N2O5)=3×10-3mol•L-1•s-1;降温至T2,反应迸行l000s时测得c(NO2)=4.98mol•L-1,则反应2N2O5(g)?4NO2(g)+O2(g)的△H<0.(填“>”、“=“或“<“).
| t(秒) | 0 | 500 | 1000 |
| N2O5浓度mol•L-1 | 5.00 | 3.50 | 2.42 |
7.对于在在标准状况下,22.4LO2中说法是正确的是( )
| A. | 物质的量不是1mol | B. | 含的氧原子个数为1mol | ||
| C. | 质子数是2mol | D. | 氧分子个数为1mol |
14.下列说法中,正确的是( )
| A. | Na2O、Na2O2为相同元素组成的金属氧化物,都属于碱性氧化物 | |
| B. | SiO2、CO2均为酸性氧化物,均能与NaOH溶液反应生成盐和水 | |
| C. | FeO、Fe2O3均为碱性氧化物,与氢碘酸反应均只发生复分解反应 | |
| D. | 将Fe(OH)3胶体和泥水分别进行过滤,分散质均不能通过滤纸孔隙 |
4.下列各项中,由实验事实能得出相应结论的是( )
| 选项 | 理由 | 结论 |
| A | 相同物质的量浓度溶液的pH: Ca(ClO)2>CH3COONa | 酸性:CH3COOH>HClO |
| B | 同体积相同pH的盐酸和醋酸与相同的锌 反应的速率:醋酸>盐酸 | 酸性:HCl>CH3COOH |
| C | 相同条件下的沸点: H2O>NH3 | 非金属性:O>N |
| D | 相同物质的量得到电子的数目: 稀硝酸>浓硝酸 | 氧化性:稀硝酸>浓硝酸 |
| A. | A | B. | B | C. | C | D. | D |
11.对H2O的电离平衡不产生影响的粒子是( )
| A. | HCl | B. | Na | C. | Na2SO4 | D. | NaHSO4 |
8.下列事故处理措施正确的是( )
| A. | 金属钠着火,立即用泡沫灭火器灭火 | |
| B. | 在气体发生装置上直接点燃甲烷气体时,必须先检验甲烷的纯度 | |
| C. | 酒精灯不慎着火,应立即吹熄 | |
| D. | 眼睛里溅进盐酸,立即用NaOH溶液洗涤眼睛 |


 ),试写出该两步反应对应的化学方程
),试写出该两步反应对应的化学方程 ;
;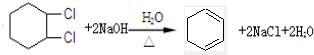 .
.