题目内容
有科学家正在研究用碳与一氧化氮反应处理环境问题:C(S)+2NO(g)?N2(g)+CO2(g);
(1)增加碳单质的量能否提高化学反应速率? .(填“可以”或“不可以”)
(2)这个反应的平衡常数表达式是 .
(3)在恒容恒温密闭容器中,科学家得到下列实验数据
请求出该应在该温度下的平衡常数K= ;达平衡时NO的转化率为 .
(4)若在反应t min后,测得NO的转化率变为40%,则此时反应是否达到平衡状态? (填是或否).判断的理由是 .
(1)增加碳单质的量能否提高化学反应速率?
(2)这个反应的平衡常数表达式是
(3)在恒容恒温密闭容器中,科学家得到下列实验数据
| 浓度(mol/L) 时间(min) | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
(4)若在反应t min后,测得NO的转化率变为40%,则此时反应是否达到平衡状态?
考点:化学平衡的影响因素,化学平衡状态的判断
专题:化学平衡专题
分析:(1)碳单质是固体,物质的量变而浓度不变;
(2)固体物质不代入平衡常数表达式;
(3)由图数据可知20min达平衡状态,平衡时生成物的浓度幂之积比上反应物浓度幂之积;
(4)根据浓度商与平衡常数的大小关系来分析解答.
(2)固体物质不代入平衡常数表达式;
(3)由图数据可知20min达平衡状态,平衡时生成物的浓度幂之积比上反应物浓度幂之积;
(4)根据浓度商与平衡常数的大小关系来分析解答.
解答:
解:(1)碳单质是固体,物质的量变而浓度不变,故答案为:不可以;
(2)固体物质不代入平衡常数表达式,所以K=
,故答案为:K=
;
(3)K=
=
=
,达平衡时NO的转化率为:
×100%=60%,故答案为;
;60%;
(4)Qc=
=
<K,所以平衡正向移动,故答案为:否;因为Qc=1/9<9/16=K,所以平衡正向移动.
(2)固体物质不代入平衡常数表达式,所以K=
| c(N2)?c(CO2) |
| c2(NO) |
| c(N2)?c(CO2) |
| c2(NO) |
(3)K=
| c(N2)?c(CO2) |
| c2(NO) |
| 0.030×0.030 |
| 0.0402 |
| 9 |
| 16 |
| 0.100-0.040 |
| 0.100 |
| 9 |
| 16 |
(4)Qc=
| 0.020×0.020 |
| 0.0602 |
| 1 |
| 9 |
点评:本题考查化学平衡常数的表达式、反应物的转化率和根据浓度商判断平衡状态的知识,比较容易.

练习册系列答案
相关题目
下列比较正确的是( )
| A、第一电离能:I1(P)>I1(S) |
| B、离子半径:r(Al3+)>r(O2-) |
| C、能量:E(4s)>E(3d) |
| D、电负性:K元素>Na元素 |
某气体的质量为3.2g,含有的是3.01×1022个分子,则该气体的相对分子质量是( )
| A、32 |
| B、64 |
| C、32 g/mol |
| D、64 g/mol |
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、1 mol?L-1NaCl溶液中含有Cl-的个数为NA |
| B、5.6g金属铁与盐酸反应失去的电子数为0.2NA |
| C、标准状况下,22.4L的水中含有的原子数为3NA |
| D、常温常压下,11.2L氯气中所含的原子数为NA |
下列叙述中,正确的是( )
| A、1 mol 乙烯分子中含有共价键的数目为7NA |
| B、1 mol甲基(-CH3)中含有电子的数目为10NA |
| C、标准状况下,1L戊烷在空气中完全燃烧生成5/22.4 L的CO2 |
| D、14 g乙烯和丙烯的混合物中含有碳原子的数目为NA |
下列反应的离子方程式正确的是( )
| A、硫酸铜溶液与烧碱溶液反应:Cu2++2OH-═Cu(OH)2↓ |
| B、石灰乳与Na2CO3溶液混合:Ca2++CO32-═CaCO3↓ |
| C、碳酸钡与硫酸反应:Ba2++SO42-═BaSO4↓ |
| D、氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-═CaSO4↓+H2O |
点豆腐所采用的凝聚剂是( )
| A、石膏 | B、硫酸钾 |
| C、氯化钡 | D、六水氯化镁 |
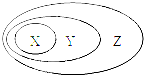 用图表示的一些物质或概念之间的从属或包含关系中,错误的是( )
用图表示的一些物质或概念之间的从属或包含关系中,错误的是( )