题目内容
下列反应的离子方程式正确的是( )
| A、硫酸铜溶液与烧碱溶液反应:Cu2++2OH-═Cu(OH)2↓ |
| B、石灰乳与Na2CO3溶液混合:Ca2++CO32-═CaCO3↓ |
| C、碳酸钡与硫酸反应:Ba2++SO42-═BaSO4↓ |
| D、氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-═CaSO4↓+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.硫酸铜溶液与烧碱溶液反应生成硫酸钠与氢氧化钡沉淀;
B.氢氧化钙为石灰乳不能拆;
C.碳酸钡为沉淀应保留化学式;
D.离子个数不符合物质的配比.
B.氢氧化钙为石灰乳不能拆;
C.碳酸钡为沉淀应保留化学式;
D.离子个数不符合物质的配比.
解答:
解:A.硫酸铜溶液与烧碱溶液反应,离子方程式:Cu2++2OH-═Cu(OH)2↓,故A正确;
B.石灰乳与Na2CO3溶液混合,离子方程式:Ca(OH)2+CO32-═CaCO3↓+2OH-,故B错误;
C.碳酸钡与硫酸反应,离子方程式:BaCO3+2H++SO42-═BaSO4↓+CO2↑+H2O,故C错误;
D.氢氧化钙溶液与等物质的量的稀硫酸混合,离子方程式:Ca2++2OH-+2H++SO42-═CaSO4↓+2H2O,故D错误;
故选:A.
B.石灰乳与Na2CO3溶液混合,离子方程式:Ca(OH)2+CO32-═CaCO3↓+2OH-,故B错误;
C.碳酸钡与硫酸反应,离子方程式:BaCO3+2H++SO42-═BaSO4↓+CO2↑+H2O,故C错误;
D.氢氧化钙溶液与等物质的量的稀硫酸混合,离子方程式:Ca2++2OH-+2H++SO42-═CaSO4↓+2H2O,故D错误;
故选:A.
点评:本题考查了离子方程式的书写,明确发生的化学反应是解题关键,注意化学式的拆分,题目难度不大.

练习册系列答案
相关题目
下列有关溶液组成的描述合理的是( )
| A、漂白粉的水溶液中大量存在:Fe2+、Cl-、Al3+、I- |
| B、强碱性溶液中可能大量存在:Na+、K+、S2-、[Al(OH)4]- |
| C、常温下pH=7的溶液中大量存在:SO42-、Na+、Cl-、Fe3+ |
| D、无色酸性溶液中可能大量存在:K+、CH3COO-、HCO3-、MnO4- |
两个体积相同的容器,一个盛有NO,一个盛有N2和O2,在同温同压下两容器内的气体一定具有相同的( )
| A、原子总数 | B、质子总数 |
| C、密度 | D、质量 |
用NA表示阿伏加德罗常数的值.下列叙述中正确的是( )
A、D
| ||
| B、相同物质的量的OH-和CH3+含有相同数目的电子 | ||
| C、NA个H2分子与0.5 NA个CO分子所占的体积比一定是2:1 | ||
| D、25℃时,pH=1的H2SO4溶液中含有H+的数目为0.2NA |
以水为分散剂的分散系,按稳定性由强到弱的顺序排列的是( )
| A、溶液、胶体、浊液 |
| B、浊液、胶体、溶液 |
| C、胶体、浊液、溶液 |
| D、浊液、溶液、胶体 |
化学兴趣小组设计如图实验装置.电解开始不久,铜电极附近溶液为无色,过了相当长时间后才呈蓝紫色.下列有关描述正确的是( )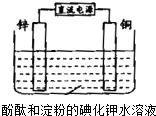

| A、电子由锌极流向铜极 |
| B、锌电极上的电极反应为:4OH--4e-═2H2O+O2↑ |
| C、铜电极实验现象的原因是生成的Cu2+和I-发生了反应 |
| D、将铜换成铁,电解开始后不久铁电极附近溶液即呈蓝紫色 |