题目内容
2.工业上可通过电解NO制备NH4NO3,其工作原理如图所示.下列说法不正确的是( )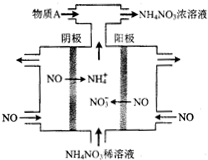
| A. | NO是常见的大气污染物之一,该装置可实现废气的治理与回收利用 | |
| B. | 阳极反应为:NO-3e-+2H2O═NO3-+4H+ | |
| C. | 阴极反应为:NO+5e-+6H+═NH4++H2O | |
| D. | 为使电解产物全部转化为NH4NO3,需向该电解池中补充水 |
分析 电解NO制备NH4NO3,阳极反应为NO-3e-+2H2O=NO3-+4H+,阴极反应为:NO+5e-+6H+=NH4++H2O,从两极反应可看出,要使得失电子守恒,阳极产生的NO3-的物质的量大于阴极产生的NH4+的物质的量,总反应方程式为:8NO+7H2O$\frac{\underline{\;通电\;}}{\;}$3NH4NO3+2HNO3,因此若要使电解产物全部转化为NH4NO3,需补充NH3,据此分析.
解答 解:电解NO制备NH4NO3,b为阳极反应为NO-3e-+2H2O=NO3-+4H+,a为阴极反应为:NO+5e-+6H+=NH4++H2O,从两极反应可看出,要使得失电子守恒,阳极产生的NO3-的物质的量大于阴极产生的NH4+的物质的量,总反应方程式为:8NO+7H2O$\frac{\underline{\;通电\;}}{\;}$3NH4NO3+2HNO3,因此若要使电解产物全部转化为NH4NO3,需补充NH3.
A.NO是常见的大气污染物之一,该装置可实现NO转化为硝酸铵,实现废气的治理与回收利用,故A正确;
B.阳极反应为:NO-3e-+2H2O=NO3-+4H+,故B正确;
C.阴极反应为:NO+5e-+6H+=NH4++H2O,故C正确;
D.要使电解产物全部转化为NH4NO3,需补充NH3,故D错误;
故选D.
点评 本题考查了电解原理的应用等,题目涉及的知识点较多,侧重于考查学生的综合运用能力,难度中等,注意基础知识的积累掌握.

练习册系列答案
相关题目
12.关于炔烃的下列描述正确的是( )
| A. | 分子里含有碳碳三键的不饱和链烃叫炔烃 | |
| B. | 炔烃分子里的所有碳原子都在同一直线上 | |
| C. | 炔烃易发生加成反应,也易发生取代反应 | |
| D. | 炔烃不能使溴水褪色,但可以使高锰酸钾酸性溶液褪色 |
13.下列化学性质中,烷烃不具备的是( )
| A. | 一定条件下发生分解反应 | B. | 可以在空气中燃烧 | ||
| C. | 光照条件下与Cl2发生取代反应 | D. | 能使酸性高锰酸钾溶液褪色 |
10.2008年北京奥运会火炬使用丙烷作燃料丙烷属于( )
| A. | 无机物 | B. | 烷烃 | C. | 氧化物 | D. | 可燃性单质 |
17.下列对物质用途的描述中,错误的是( )
| A. | 浓硫酸可用于干燥NH3、H2、O2等气体 | |
| B. | 二氧化硫可用来漂白纸浆、毛、丝等 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 干冰升华没有断裂化学键 |
7.下列事实及解释的化学(或离子)方程式均正确的是( )
| A. | MnCl2溶液中常含有Cu2+,可添加难溶电解质MnS除去:Cu2++S2-=CuS↓ | |
| B. | 盛放NaOH溶液的试剂瓶不能用玻璃塞是因为:SiO2+2OH-=SiO32-+H2O | |
| C. | 向FeBr2溶液中通入足量氯气:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 向氨水中滴入少量饱和氯化铁溶液制各Fe(OH)3胶体:Fe3++3NH3•H2O?Fe(OH)3(胶体)+3NH4+ |
14.有A、B、C、D四块金属,若A、B用导线相连成原电池时,A为负极;若C、D相连构成原电池时,电流由D流向C;A、C相连浸入稀硫酸中时,C极上产生大量气泡;把D投入到B的硫酸盐溶液中,D的表面有B析出;则四种金属的活动性顺序为( )
| A. | B>D>C>A | B. | C>A>B>D | C. | A>C>D>B | D. | A>B>C>D |
11.取相同体积的KI、Na2S、FeBr2溶液,分别通入足量氯气,当反应恰好完成时三种溶液消耗氯气的体积相同(同温,同压条件下).则KI、Na2S、FeBr2溶液的物质的量浓度之比为( )
| A. | 6:3:2 | B. | 1:2:3 | C. | 3:6:2 | D. | 2:1:3 |
10.下列实验操作中正确的是( )
| A. | 蒸发结晶时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 过滤时,溶液的液面高于滤纸的边缘 | |
| C. | 分液操作时,下层液体从分液漏斗下口放出后,再将上层液体从上口倒到另一个烧杯中 | |
| D. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |