题目内容
7.下列事实不能用勒夏特列原理解释的是( )| A. | 光照新制的氯水时,溶液的pH逐渐减小 | |
| B. | 可用浓氯水和氢氧化钠固体快速制取氨气 | |
| C. | 增大压强,有利于SO2与O2反应生成SO3 | |
| D. | 硅酸钠溶液在保存时不应用玻璃塞 |
分析 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动,使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用.
解答 解:A.氯水中存在化学平衡Cl2+H2O?HCl+HClO,光照使氯水中的次氯酸分解,次氯酸浓度减小,使得平衡向右移动,氢离子浓度变大,溶液的PH值减小,能用勒夏特列原理解释,故A不选;
B.氨水中存在氨气的溶解平衡,氢氧化钠溶解放出热量,升高温度抑制氨气溶解,从而生成氨气,可以用平衡移动原理解释,故B不选;
C.二氧化硫与氧气生成三氧化硫的反应为气体体积缩小的反应,增大压强平衡向着正向移动,有利于三氧化硫的生成,可以用平衡移动原理解释,故C不选;
D.硅酸钠具有粘性,保存在有玻璃塞的试剂瓶中,会把玻璃粘在一起,与勒夏特列原理没有关系,故D选;
故选D.
点评 本题考查了勒夏特列原理的应用,题目难度不大,明确勒夏特列原理的内容为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
17.将4mol A气体和2mol B气体在1L的容器中混合,并在一定条件下发生如下反应:2A(g)+B(g)?2C(g),若是2min后测得A的浓度为2mol/L,物质A表示的反应速率正确的是( )
| A. | 2mol/L•min | B. | 1 mol/L•min | C. | 0.5 mol/L•min | D. | 0.6 mol/L•min |
18.下列说法中正确的是( )
| A. | 烃是指含有碳、氢元素的有机物 | |
| B. | 燃烧后能产生CO2和H2O的有机物一定是烃 | |
| C. | 天然气、沼气、坑气、煤气的主要成分都是甲烷 | |
| D. | 形成化合物种类最多的元素位于周期表中第二周期第IVA族 |
15.生活中的如图制品没有用到高分子材料的是( )
| A. |  电话卡 | B. |  塑料袋 | C. |  不锈钢锅 | D. |  尼龙雨衣 |
2.向等物质的量浓度的NaOH和Na2CO3的混合溶液中加入稀盐酸.下列离子方程式与事实不相符的是( )
| A. | OH-+CO32-+2H+═HCO3-+H2O | B. | 2OH-+CO32-+3H+═HCO3-+2H2O | ||
| C. | OH-+CO32-+3H+═CO2↑+2H2O | D. | 2OH-+CO32-+4H+═CO2↑+3H2O |
12.向淀粉溶液中加入少量的稀硫酸并加热,使淀粉发生水解,为测定其水解程度,需要下列试剂中的( )
①氢氧化钠溶液;②银氨溶液;③新制氢氧化铜悬浊液;④碘水;⑤氯化钡溶液.
①氢氧化钠溶液;②银氨溶液;③新制氢氧化铜悬浊液;④碘水;⑤氯化钡溶液.
| A. | ①④⑤ | B. | ①③④ | C. | ②③④ | D. | ①②③ |
19.a、b、c、d为短周期元素,a的原子中只有1个电子,b2-和c+离子的电子层结构相同,d与b同族.下列叙述错误的是( )
| A. | c的原子半径是这些元素中最大的 | |
| B. | b与其他三种元素均可形成至少两种二元化合物 | |
| C. | a与其他三种元素形成的二元化合物中其化合价均为+1 | |
| D. | d和a形成的化合物的溶液呈弱酸性 |
11.有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:

部分实验现象(1)中 a极质量减小,b极质量增加,(2)中 b极有气体产生,c极无变化,(3)中d极溶解,c极有气体产生,(4)中 电流计指示在导线中,电流从a极流向d极
由此可判断这四种金属的活动性顺序是( )

部分实验现象(1)中 a极质量减小,b极质量增加,(2)中 b极有气体产生,c极无变化,(3)中d极溶解,c极有气体产生,(4)中 电流计指示在导线中,电流从a极流向d极
由此可判断这四种金属的活动性顺序是( )
| A. | a>b>c>d | B. | b>c>d>a | C. | d>a>b>c | D. | a>b>d>c |
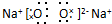 ,甲中的化学键类型为离子键、共价键.
,甲中的化学键类型为离子键、共价键.