题目内容
19.a、b、c、d为短周期元素,a的原子中只有1个电子,b2-和c+离子的电子层结构相同,d与b同族.下列叙述错误的是( )| A. | c的原子半径是这些元素中最大的 | |
| B. | b与其他三种元素均可形成至少两种二元化合物 | |
| C. | a与其他三种元素形成的二元化合物中其化合价均为+1 | |
| D. | d和a形成的化合物的溶液呈弱酸性 |
分析 a、b、c、d为短周期元素,a的原子中只有1个电子,则a为H元素,b2-和c+离子的电子层结构相同,则b为O元素,c为Na;d与b同族,则d为S元素,结合元素周期律与元素化合物性质解答.
解答 解:a、b、c、d为短周期元素,a的原子中只有1个电子,则a为H元素,b2-和c+离子的电子层结构相同,则b为O元素,c为Na;d与b同族,则d为S元素.
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,四种元素中Na的原子半径最大,故A正确;
B.O元素与氢元素形成H2O、H2O2,与Na形成Na2O、Na2O2,与硫形成SO2、SO3,故B正确;
C.氢与钠形成的化合物NaH中氢元素化合价为-1价,故C错误;
D.d和a形成的化合物为H2S,其溶液呈弱酸性,故D正确.
故选:C.
点评 本题考查结构性质位置关系应用,注意抓住短周期元素进行推断,熟练掌握元素周期律与元素化合物知识.

练习册系列答案
相关题目
9.苯的结构式可用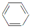 来表示,下列关于苯的叙述中正确的是( )
来表示,下列关于苯的叙述中正确的是( )
 来表示,下列关于苯的叙述中正确的是( )
来表示,下列关于苯的叙述中正确的是( )| A. | 苯是无色无味,密度比水大的液体 | |
| B. | 苯中含有碳碳双键,所以苯属于烯烃 | |
| C. | 苯分子中6个碳碳化学键完全相同 | |
| D. | 苯可以与溴水、高锰酸钾溶液反应而使它们褪色 |
10.下列有关化学用语能确定为丙烯的是( )
| A. | CH2═CHCH3 | B. | C3H6 | C. | 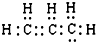 | D. | CH2═CH3CH |
7.下列事实不能用勒夏特列原理解释的是( )
| A. | 光照新制的氯水时,溶液的pH逐渐减小 | |
| B. | 可用浓氯水和氢氧化钠固体快速制取氨气 | |
| C. | 增大压强,有利于SO2与O2反应生成SO3 | |
| D. | 硅酸钠溶液在保存时不应用玻璃塞 |
8. 一定温度下,密闭容器内某一反应中X、Y的物质的量随反应时间变化的曲线如图所示,下列叙述中不正确的是( )
一定温度下,密闭容器内某一反应中X、Y的物质的量随反应时间变化的曲线如图所示,下列叙述中不正确的是( )
 一定温度下,密闭容器内某一反应中X、Y的物质的量随反应时间变化的曲线如图所示,下列叙述中不正确的是( )
一定温度下,密闭容器内某一反应中X、Y的物质的量随反应时间变化的曲线如图所示,下列叙述中不正确的是( )| A. | 反应的化学方程式为:2X?Y | B. | t1时,Y的浓度是X浓度的2倍 | ||
| C. | t2时,正反应速率大于逆反应速率 | D. | t3时,正逆反应速率相等,达到平衡 |
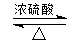
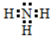 ;实验室制备气体A的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
;实验室制备气体A的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.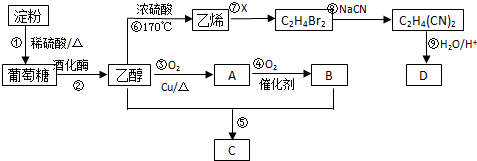
 CH3COOCH2CH3+H2O.反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是NaOH溶液.
CH3COOCH2CH3+H2O.反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是NaOH溶液.
 .
.