题目内容
工业上制取ClO2的化学反应:2NaClO3+SO2+H2SO4═2ClO2+2NaHSO4,下列说法中正确的是( )
| A、NaClO3在反应中失去电子 |
| B、SO2在反应中被氧化 |
| C、H2SO4在反应中作氧化剂 |
| D、1 mol氧化剂在反应中得到2 mol电子 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:反应中Cl元素由+5价降低到+4价,被还原,NaClO3为氧化剂,S元素化合价由+4价升高到+6价,被氧化,SO2为还原剂,结合化合价的变化解答该题.
解答:
解:A.NaClO3在反应中Cl元素由+5价降低到+4价,得电子,被还原,故A错误;
B.SO2在反应中S元素化合价由+4价升高到+6价,失电子,被氧化,故B正确;
C.H2SO4在反应中没有参与氧化还原反应,仅起到酸性的作用,故C错误;
D.反应中Cl元素由+5价降低到+4价,则1mol氧化剂在反应中得到1mol电子,故D错误.
故选B.
B.SO2在反应中S元素化合价由+4价升高到+6价,失电子,被氧化,故B正确;
C.H2SO4在反应中没有参与氧化还原反应,仅起到酸性的作用,故C错误;
D.反应中Cl元素由+5价降低到+4价,则1mol氧化剂在反应中得到1mol电子,故D错误.
故选B.
点评:本题考查氧化还原反应,侧重于学生的分析能力的考查,注意从元素化合价的角度认识相关概念和物质的性质,难度不大.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
正确掌握好化学用语是学好化学的基础,下列有关表述正确的是( )
A、Na+结构示意图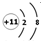 | ||||
B、质量数为16的氧原子:
| ||||
| C、纯碱的化学式:NaHCO3 | ||||
D、铁丝在氯气中燃烧的化学方程式:Fe+Cl2
|
科学家发现了如下反应:O2+PtF6═O2(PtF6),已知O2(PtF6)为离子化合物,Pt为+5价,下列说法正确的是( )
| A、O和F无正化合价 |
| B、1mol O2参加反应,转移1mol e- |
| C、上述反应中O2作氧化剂 |
| D、上述反应属于加成反应 |
工业上冶炼锡的第一步反应原理为2SnO2+3C═2Sn+aM↑+CO2↑,则下列说法中错误的是( )
| A、反应中SnO2被还原 |
| B、a的值为3 |
| C、反应后元素化合价升高生成的物质有两种 |
| D、每生成1mol CO2转移电子8 mol |
下列各组离子可以大量共存的是( )
| A、Al3+、Fe3+、Br-、SO42- |
| B、K+、Ca2+、SO42-、Cl- |
| C、H+、Cu2+、I-、NO3- |
| D、Al3+、Mg2+、NO3-、HCO3- |
下列离子方程式书写正确的是( )
| A、向氯化铝溶液中加入足量氨水:Al3++4NH3?H2O═AlO2-+2H2O+4NH4+ |
| B、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
| C、三氯化铁溶液中加入铁粉:Fe3++Fe═2Fe2+ |
| D、FeCl2溶液跟Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |

 经两步反应制得,写出第一步反应的化学方程式
经两步反应制得,写出第一步反应的化学方程式