题目内容
5.下列说法错误的是( )| A. | 乙醇和乙酸都是常用调味品的主要成分 | |
| B. | 乙醇和乙酸的沸点和熔点都比C2H6和C2H4的沸点和熔点高 | |
| C. | 乙酸和乙醇之间能发生酯化反应 | |
| D. | 乙醇 和乙酸都能发生消去反应 |
分析 乙醇含有羟基,可发生取代、消去和氧化反应,乙酸含有羧基,具有酸性,可发生中和、酯化反应,二者都可作为调味品的主要成分,以此解答该题.
解答 解:A.乙酸为食醋的主要成分,乙醇为料酒的主要成分,二者都是常用调味品的主要成分,故A正确;
B.乙酸、乙醇常温下为液体,存在分子间氢键,沸点较高,而C2H6和C2H4常温下为气体,沸点较低,故B正确;
C.乙酸含有羧基、乙醇含有羟基,二者可发生酯化反应生成乙酸乙酯,故C正确;
D.乙酸不能发生消去反应,故D错误.
故选D.
点评 本题考查有机物的结构和性质,为高频考点,侧重考查乙酸、乙醇的结构、性质和用途,主要把握物质的结构和官能团的性质,题目有利于培养学生良好的科学素养,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列装置的示意图均与电化学相关,有关叙述正确的是( ) 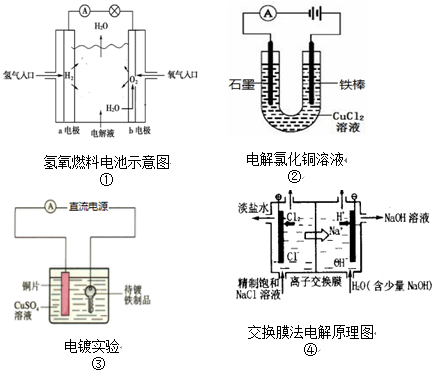

| A. | 装置①中,b极发生氧化反应 | |
| B. | 装置②中,铁棒上析出红色固体 | |
| C. | 装置③中,若电镀前两极金属的质量相等,电镀完成后二者质量差5.12g,则电镀时电路中的待镀铁制品应与电源负极相连,外电路转移的电子数为0.08mol | |
| D. | 装置④中,离子交换膜应为阴离子交换膜 |
13.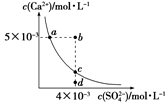 常温下,Ksp(CaSO4)=9×10-6,CaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
常温下,Ksp(CaSO4)=9×10-6,CaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
 常温下,Ksp(CaSO4)=9×10-6,CaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
常温下,Ksp(CaSO4)=9×10-6,CaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )| A. | CaSO4在稀硫酸中的溶解性比在纯水中的溶解性强 | |
| B. | a点对应的Ksp等于c点对应的Ksp | |
| C. | d点溶液通过蒸发可以变到c点 | |
| D. | b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×10-3mol/L |
10.将相同状况下等体积的SO2和Cl2充分混合后,通入加有品红的氯化钡溶液,可观察到的现象是( )
| A. | 褪色但无沉淀 | B. | 不褪色但有沉淀 | ||
| C. | 褪色且有沉淀 | D. | 不褪色也没有沉淀 |
17.根据所给的信息和标志,判断下列说法错误的是( )
| A | B | C | D |
 | 碳酸氢钠药片 |  |  |
| 如图为铝热反应的实验装置,工业上利用铝热反应大量冶炼金属铁 | 如图现象为丁达尔效应,丁达尔效应可用于鉴别溶液和胶体 | 如图药品属抗酸药,可治疗胃酸过多 | 看到有该标志的丢弃物,应远离并报警 |
| A. | A | B. | B | C. | C | D. | D |
14.下列有关说法正确的是( )
| A. | 石油裂解和油脂皂化都是由高分子生成小分子的过程 | |
| B. | 乙烷、苯、裂化汽油均不能使酸性高锰酸钾溶液褪色 | |
| C. | 甲苯的硝化、乙酸乙酯的水解均可看作是取代反应 | |
| D. | 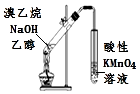 如图装置可以用于检验溴丙烷的消去产物 |
2.实验中不能直接测出由石墨和氢气生成甲烷反应的△H,已知下列数据:
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ•mol-1
C(石墨)+O2(g)=CO2(g)△H=-393•5kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ•mol-1
则C(石墨)+2H2(g)=CH4(g) 的△H是( )
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ•mol-1
C(石墨)+O2(g)=CO2(g)△H=-393•5kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ•mol-1
则C(石墨)+2H2(g)=CH4(g) 的△H是( )
| A. | -74.8 kJ•mol-1 | B. | +74.8 kJ•mol-1 | C. | -211.0 kJ•mol-1 | D. | +211.0 kJ•mol-1 |