题目内容
10.将相同状况下等体积的SO2和Cl2充分混合后,通入加有品红的氯化钡溶液,可观察到的现象是( )| A. | 褪色但无沉淀 | B. | 不褪色但有沉淀 | ||
| C. | 褪色且有沉淀 | D. | 不褪色也没有沉淀 |
分析 根据SO2具有还原性,Cl2具有氧化性,二者发生的氧化还原反应SO2+Cl2+2H2O═H2SO4+2HCl,结合生成物的性质解答.
解答 解:因SO2具有还原性,Cl2具有氧化性,则等体积的SO2和Cl2充分混合发生SO2+Cl2+2H2O═H2SO4+2HCl,又SO2和Cl2都没有剩余,则不能使品红褪色,生成的硫酸与氯化钡反应生成白色的硫酸钡沉淀,
故选:B.
点评 本题考查氯气、二氧化硫的性质,熟悉二者等物质的量混合发生的氧化还原反应是解答本题的关键,难度不大.

练习册系列答案
相关题目
20.下列溶液中n(Cl-) 与50mL 1mol/L 氯化铝溶液中的n(Cl-) 相等的是( )
| A. | 150 mL 1mol/L 氯化钠溶液 | B. | 75 mL 2mol/L 氯化镁溶液 | ||
| C. | 150 mL 2mol/L氯化铵溶液 | D. | 50 mL 3mol/L 氯化铁溶液 |
1.下列有关物质用途的说法中,不正确的是( )
| A. | 乙酸可以做调味剂 | B. | 油脂可用来制造肥皂 | ||
| C. | 乙烯可用作水果催熟剂 | D. | 工业酒精可用于勾兑白酒 |
18.下列说法正确的一组是( )
①不溶于水的盐(CaC03、BaSO4等)部是弱电解质
②CO2和HCl都是化合物又是电解质
③0.5mol/L所有一元酸中氢离子浓度部是0.5mol/L
④强酸溶液中氢离子浓度一定大于弱酸溶液中氢离子浓度
⑤电解质溶液导电的原因是溶液中有自由移动的阴阳离子
⑥熔融的电解质都能导电.
①不溶于水的盐(CaC03、BaSO4等)部是弱电解质
②CO2和HCl都是化合物又是电解质
③0.5mol/L所有一元酸中氢离子浓度部是0.5mol/L
④强酸溶液中氢离子浓度一定大于弱酸溶液中氢离子浓度
⑤电解质溶液导电的原因是溶液中有自由移动的阴阳离子
⑥熔融的电解质都能导电.
| A. | ①③⑤⑥ | B. | ②④⑤⑥ | C. | 只有⑤ | D. | 只有⑤⑥ |
5.下列说法错误的是( )
| A. | 乙醇和乙酸都是常用调味品的主要成分 | |
| B. | 乙醇和乙酸的沸点和熔点都比C2H6和C2H4的沸点和熔点高 | |
| C. | 乙酸和乙醇之间能发生酯化反应 | |
| D. | 乙醇 和乙酸都能发生消去反应 |
15.研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果.下列表达不正确的是( )
| A. | 分散质粒子直径与分散系种类: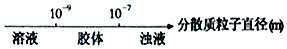 | |
| B. | NaOH溶液与CO2反应后溶液中的钠盐: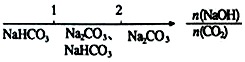 | |
| C. | AlCl3溶液中滴加NaOH溶液后铝的存在形式: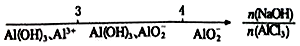 | |
| D. | Na与O2反应的产物: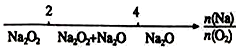 |
2.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 30g乙烷所含共用电子对数目为6NA | |
| B. | 标准状况下,22.4L已烷中共价键数目为6NA | |
| C. | 14g乙烯和丁烯的混合物中含有的原子总数为3NA个 | |
| D. | 2.8g聚乙烯中含有的碳原子数为0.1NA |
19.下列各组液体混合物,能用分液漏斗分离的是( )
| A. | 1,2-二溴乙烷和四氯化碳 | B. | 己烷和高锰酸钾溶液 | ||
| C. | 氯仿和异戊烷 | D. | 酒精和水 |