题目内容
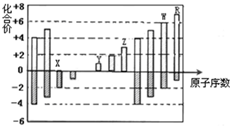 如图所示是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
如图所示是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )| A、原子半径:Z>Y>X |
| B、气态氢化物的还原性:W>R |
| C、WX3和水反应形成的化合物是离子化合物 |
| D、含Z的盐溶液一定显示酸性 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:由表中化合价可知,X的化合价为-2价,没有正化合价,故X为O元素,Y的化合价为+2价,处于ⅡA族,原子序数大于O元素,故Y为Mg元素,Z为+3价,为Al元素,W的化合价为+6、-2价,故W为S元素,R的最高正价为+7价,应为Cl元素,结合对应单质、化合物的性质以及题目要求解答该题.
解答:
解:由表中化合价可知,X的化合价为-2价,没有正化合价,故X为O元素,Y的化合价为+2价,处于ⅡA族,原子序数大于O元素,故Y为Mg元素,Z为+3价,为Al元素,W的化合价为+6、-2价,故W为S元素,R的最高正价为+7价,应为Cl元素,
A.已知X为O,Y为Na,Z为Al,所以原子半径应为Na>Al>O,故A错误;
B.已知W为S,R为Cl,所以非金属性Cl>S,则气态氢化物的还原性S>Cl,故B正确;
C.X为O,W为S,所以WX3和水反应形成的化合物是硫酸,是共价化合物,故C错误;
D.Z为Al,如为NaAlO2,则溶液呈碱性,故D错误.
故选B.
A.已知X为O,Y为Na,Z为Al,所以原子半径应为Na>Al>O,故A错误;
B.已知W为S,R为Cl,所以非金属性Cl>S,则气态氢化物的还原性S>Cl,故B正确;
C.X为O,W为S,所以WX3和水反应形成的化合物是硫酸,是共价化合物,故C错误;
D.Z为Al,如为NaAlO2,则溶液呈碱性,故D错误.
故选B.
点评:本题考查结构性质与位置关系、元素周期律等,侧重于学生的分析能力的考查,难度不大,根据推断元素是解题的关键,根据化合价结合原子序数进行推断.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列离子反应方程式能正确表达相关反应的是( )
| A、在FeBr2溶液中通入足量氯气:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | ||||
B、用石墨电极电解氯化镁溶液:2Cl-+2H2O
| ||||
| C、向CaCl2溶液中通入CO2气体:Ca2++CO2+H2O═CaCO3↓+2H+ | ||||
| D、等物质的量浓度的小苏打溶液和石灰水按体积比3:2混合:3HCO3-+2Ca2++3OH-═2CaCO3↓+CO32-+3H2O |
如图装置能达到实验目的是( )


| A、用图①所示装置测定NaOH的浓度 |
| B、用图②所示装置分馏少量石油 |
| C、用图③所示装置在实验室制备收集氨气 |
| D、用图④所示装置鉴别碳酸钠和碳酸氢钠 |
实验室制备下列气体时,所用方法正确的是( )
| A、制氧气时,用Na2O2或H2O2作反应物可选择相同的气体发生装置 |
| B、制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体 |
| C、制乙烯时,用排水法或向上排空气法收集气体 |
| D、制二氧化氮时,用水或NaOH溶液吸收尾气 |
下列反应的离子方程式正确的是( )
A、硫酸氢铵溶液与足量氢氧化钠溶液反应:NH4++OH-
| ||||
B、将饱和FeCl3溶液滴入沸水中制备胶体:Fe3++3H2O
| ||||
| C、Fe2O3固体溶于过量氢碘酸溶液中:Fe2O3+6H+═2Fe3++3H2O | ||||
| D、苯酚钠溶液中通入少量的CO2:2C2H5O-+CO2+H2O→2C2H5OH+CO32- |

 氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.
氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.