题目内容
实验室制备下列气体时,所用方法正确的是( )
| A、制氧气时,用Na2O2或H2O2作反应物可选择相同的气体发生装置 |
| B、制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体 |
| C、制乙烯时,用排水法或向上排空气法收集气体 |
| D、制二氧化氮时,用水或NaOH溶液吸收尾气 |
考点:真题集萃,气体的收集,常见气体制备原理及装置选择
专题:实验题
分析:A.Na2O2与水反应,H2O2在二氧化锰催化条件下都能制取氧气,二者都是固体与液体反应;
B.HCl气体能与碳酸氢钠反应生成CO2,引入新的杂质气体;
C.乙烯的密度与空气接近;
D.二氧化氮与水反应生成一氧化氮.
B.HCl气体能与碳酸氢钠反应生成CO2,引入新的杂质气体;
C.乙烯的密度与空气接近;
D.二氧化氮与水反应生成一氧化氮.
解答:
解:A.Na2O2与水反应,H2O2在二氧化锰催化条件下都能制取氧气,二者都是固体与液体常温条件下反应,可选择相同的气体发生装置,故A正确;
B.实验室制取氯气含有氯化氢和水分,常用饱和食盐水和浓硫酸净化气体,若饱和NaHCO3溶液,HCl会和NaHCO3反应生成CO2,引入新的杂质,故B错误;
C.乙烯的密度与空气接近,不能用排空气法收集,故C错误;
D.二氧化氮与水反应生成一氧化氮,仍然污染空气,所以不能用水吸收,故D错误.
故选A.
B.实验室制取氯气含有氯化氢和水分,常用饱和食盐水和浓硫酸净化气体,若饱和NaHCO3溶液,HCl会和NaHCO3反应生成CO2,引入新的杂质,故B错误;
C.乙烯的密度与空气接近,不能用排空气法收集,故C错误;
D.二氧化氮与水反应生成一氧化氮,仍然污染空气,所以不能用水吸收,故D错误.
故选A.
点评:本题考查气体的制备与收集,题目难度中等,解答本题的关键是把握相关物质的性质,学习中注意积累.

练习册系列答案
相关题目
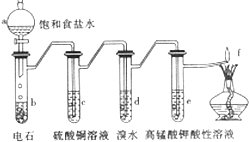 如图是制备和研究乙炔性质的实验装置图.下列说法不正确的是( )
如图是制备和研究乙炔性质的实验装置图.下列说法不正确的是( )| A、制备乙炔的反应原理是:CaC2+2H2O→Ca(OH)2+C2H2↑ |
| B、c的作用是除去影响后续实验的杂质 |
| C、d中的有机产物与AgNO3溶液混合能产生沉淀 |
| D、e中的现象说明乙炔能被高锰酸钾酸性溶液氧化 |
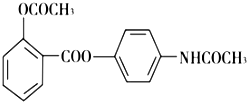 贝诺酯具有抗风湿、解热镇痛作用,其结构简式如图,下列说法正确的是( )
贝诺酯具有抗风湿、解热镇痛作用,其结构简式如图,下列说法正确的是( )| A、贝诺酯可与水任意比互溶 |
| B、贝诺酯完全水解后能得到3种物质 |
| C、1mol贝诺酯最多可与9mol H2发生加成反应 |
| D、贝诺酯可发生取代反应、消去反应和聚合反应 |
下列说法不正确的是( )
| A、分子式为CH4O和C2H6O的物质不一定互为同系物 |
| B、通过乙烷的取代反应或乙烯的加成反应都可以制取纯净的氯乙烷 |
| C、淀粉.纤维素都属于糖类,它们通式相同,但它们不互为同分异构体 |
| D、某有机化合物仅由C.H.O三种元素组成,其相对分子质量小于150,若已知其中氧的质量分数为50%,则分子中碳原子的个数最多为5 |
下列说法正确的是( )
| A、钙和氮均为人体所需的微量元素 |
| B、二氧化硅是太阳能电池的主要材料 |
| C、油脂和蛋白质均属于高分子化合物 |
| D、明矾与水作用能生成有吸附性的物质 |
下列对应关系正确的是( )
| A | B | C | D |
 |
 |
 |
 |
| 浓硫酸 | 氢氧化钠 | 废旧灯管 | 废旧易拉罐 |
| A、A | B、B | C、C | D、D |
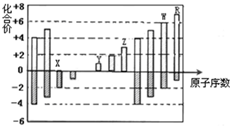 如图所示是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
如图所示是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )| A、原子半径:Z>Y>X |
| B、气态氢化物的还原性:W>R |
| C、WX3和水反应形成的化合物是离子化合物 |
| D、含Z的盐溶液一定显示酸性 |
下列各组离子在水溶液中能大量共存的是( )
| A、Na+、HCO3-、SO32-、OH- |
| B、Al3+、H+、SiO32-、I- |
| C、Fe2+、K+、NO3-、SO42- |
| D、Fe3+、NH4+、ClO-、CO32- |
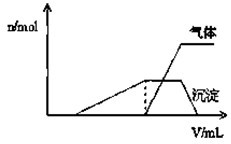 1L某混合溶液,可能含有的离子如下表:
1L某混合溶液,可能含有的离子如下表: