题目内容
关注饮用水,保证人民的生活质量.回答下列两个问题:
(1)饮用水中的 NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,可以在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O.请回答下列问题:
①上述反应中 元素的化合价升高,则该元素的原子 (填“得到”或“失去”)电子.
②用“双线桥法”表示反应中电子转移的方向和数目:
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O
(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一.漂白粉是常用的消毒剂.
①工业上将氯气通入石灰乳制取漂白粉,化学方程式为 .
②漂白粉的有效成分是(填化学式) .
③漂白粉溶于水后,受空气中的CO2作用,即产生漂白、杀菌作用,离子方程式为 .
(1)饮用水中的 NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,可以在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O.请回答下列问题:
①上述反应中
②用“双线桥法”表示反应中电子转移的方向和数目:
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O
(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一.漂白粉是常用的消毒剂.
①工业上将氯气通入石灰乳制取漂白粉,化学方程式为
②漂白粉的有效成分是(填化学式)
③漂白粉溶于水后,受空气中的CO2作用,即产生漂白、杀菌作用,离子方程式为
考点:氧化还原反应,氯、溴、碘及其化合物的综合应用
专题:氧化还原反应专题,元素及其化合物
分析:(1)反应10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O中,Al元素化合价升高,被氧化,N元素化合价降低,被还原,结合化合价的变化判断电子的得失以及电子转移的方向和数目;
(2)①氯气和石灰乳反应生成氯化钙、次氯酸钙和水;
②漂白粉的有效成分为次氯酸钙;
③漂白粉和二氧化碳、水反应生成碳酸钙沉淀和次氯酸.
(2)①氯气和石灰乳反应生成氯化钙、次氯酸钙和水;
②漂白粉的有效成分为次氯酸钙;
③漂白粉和二氧化碳、水反应生成碳酸钙沉淀和次氯酸.
解答:
解:(1)①反应10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O中,Al元素化合价升高,被氧化,在反应中失去电子,
故答案为:Al;失去;
②反应中铝失去电子数为10×3,NaNO3得到电子数为6×5,所以用“双线桥法”标明反应中电子转移的方向和数目为: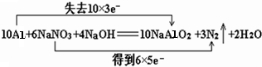 ,
,
故答案为: .
.
(2)①石灰乳和氯气反应制备漂白粉,该反应为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
②由2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O可知,生成物中CaCl2和Ca(ClO)2为漂白粉的主要成分,Ca(ClO)2为有效成分,
故答案为:Ca(ClO)2;
③漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,反应的离子方程式为:Ca2++2ClO-+CO2+H2O═CaCO3↓+2 HClO;
故答案为:Ca2++2 ClO-+CO2+H2O═CaCO3↓+2HClO.
故答案为:Al;失去;
②反应中铝失去电子数为10×3,NaNO3得到电子数为6×5,所以用“双线桥法”标明反应中电子转移的方向和数目为:
 ,
,故答案为:
 .
.(2)①石灰乳和氯气反应制备漂白粉,该反应为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
②由2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O可知,生成物中CaCl2和Ca(ClO)2为漂白粉的主要成分,Ca(ClO)2为有效成分,
故答案为:Ca(ClO)2;
③漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,反应的离子方程式为:Ca2++2ClO-+CO2+H2O═CaCO3↓+2 HClO;
故答案为:Ca2++2 ClO-+CO2+H2O═CaCO3↓+2HClO.
点评:本题考查了氧化还原反应的特征分析,电子转移的计算应用,工业制备物质的原理分析判断,把握氯气的性质、次氯酸钙的性质、HClO的性质为解答的关键,明确发生的化学反应即可解答,题目难度不大.

练习册系列答案
相关题目
某固体A在一定条件下加热分解,产物全是气体,A的分解反应为:2A
B↑+2C↑+2D↑,现测得分解产生的混合气体对氢气的相对密度为d,则A的相对分子质量为( )
| ||
| A、2d | B、10d |
| C、5d | D、0.8d |
废电池必须进行集中处理的主要原因是( )
| A、利用电池外壳的金属材料 |
| B、防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 |
| C、防止电池中渗泄的电解液腐蚀其他物品 |
| D、回收其中的石墨电极 |
某无色酸性溶液中,则该溶液中一定能够大量共存的离子组是( )
| A、Fe2+、Ba2+、NO3-、Cl- |
| B、Na+、NH4+、SO42-、Cl- |
| C、Na+、K+、SO32-、NO3- |
| D、Na+、K+、MnO4-、Br- |
分子式为C5H11Br的一溴代烷水解后的产物在红热铜丝催化,最多可能被空气氧化生成的醛的种数是( )
| A、2种 | B、3种 | C、4种 | D、5种 |

 在①CO2、②NO2、③CO、④Cl2、⑤HCl、⑥NH3等气体中(选填序号)
在①CO2、②NO2、③CO、④Cl2、⑤HCl、⑥NH3等气体中(选填序号)