题目内容
4.下列说法正确的是( )| A. | 甲烷的标准燃烧热为-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 Mpa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的△H不同 | |
| D. | 101 kPa时,硫的标准燃烧热与硫完全燃烧时的物质的量无关 |
分析 A.燃烧热中水为液态;
B.合成氨为可逆反应,热化学方程式中为完全转化时的能量变化;
C.焓变与反应条件无关;
D.燃烧热为1mol纯物质完全燃烧生成稳定氧化物时的能量变化.
解答 解:A.甲烷的标准燃烧热为-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式表示为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3 kJ•mol-1,故A错误;
B.500℃、30 Mpa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,为可逆反应,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H<-38.6kJ•mol-1,故B错误;
C.焓变与反应条件无关,则同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的△H相同,故C错误;
D.燃烧热为1mol纯物质完全燃烧生成稳定氧化物时的能量变化,则101 kPa时,硫的标准燃烧热与硫完全燃烧时的物质的量无关,故D正确;
故选D.
点评 本题考查热化学方程式,为高频考点,把握焓变与反应条件、反应中能量变化为解答该题的关键,侧重分析与应用能力的考查,注意燃烧热的判断,题目难度不大.

练习册系列答案
相关题目
5.下列反应中,不能说明CO2是酸性氧化物的是( )
| A. | Na2CO3+H2SO4═CO2↑+H2O+Na2SO4 | B. | CO2+2NaOH═Na2CO3+H2O | ||
| C. | CO2+2Mg$\frac{\underline{\;点燃\;}}{\;}$ 2MgO+C | D. | CO2+Na2O=Na2CO3 |
3.在某无色透明的酸性溶液中,能共存的离子组是( )
| A. | Na+、Mg2+、Cl-、OH- | B. | H+、Ca2+、Na+、NO3- | ||
| C. | Cu2+、K+、SO42-、NO3- | D. | Na+、SO42-、OH-、Ca2+ |
9.燃烧a g乙醇(液),生成二氧化碳气体和液态水,放出的热量为Q kJ,经测定,生成的CO2与足量澄清石灰水反应得到5g沉淀,则乙醇燃烧的热化学方程式是( )
| A. | C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1)△H=-20Q kJ/mol | |
| B. | C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(l)△H=-40Q kJ/mol | |
| C. | $\frac{1}{2}$C2H5OH(1)+$\frac{3}{2}$O2(g)=CO2(g)+$\frac{3}{2}$H2O(g)△H=-20Q kJ/mol | |
| D. | C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(g)△H=-40Q kJ/mol |
16.下列属于热化学方程式的是( )
| A. | C+O2$\stackrel{点燃}{→}$CO2 | B. | C(s)+O2(g)$\stackrel{点燃}{→}$CO2(g)+393.5kJ | ||
| C. | C(s)+O2(g)$\stackrel{点燃}{→}$CO2(g) | D. | C(s)+O2(g)=CO2(g)+393.5kJ |
14.用稀的碱性溶液或清水浸泡,可使残留在蔬菜上的农药降低毒性.如用碱性溶液浸泡蔬菜,可在水中加入适量的( )
| A. | 白酒 | B. | 纯碱 | C. | 白糖 | D. | 食醋 |
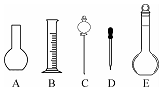 某同学通过实验研究钠及其化合物的有关性质,请回答相关问题.
某同学通过实验研究钠及其化合物的有关性质,请回答相关问题. :3-甲基-3-戊醇
:3-甲基-3-戊醇 :4-甲基-2-戊烯
:4-甲基-2-戊烯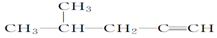 :4-甲基-1-戊炔
:4-甲基-1-戊炔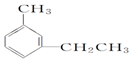 :1-甲基-3-乙苯(或间甲乙苯).
:1-甲基-3-乙苯(或间甲乙苯).