题目内容
10.用质量分数98%、密度为1.84g•cm-3的浓硫酸配制480mL0.92mol•L-1的稀硫酸(1)配制时,除量筒、烧杯、玻璃棒外还需玻璃仪器有胶头滴管、500mL容量瓶.
(2)减小误差量取时需选用合适的量筒量取25.0mL浓硫酸
(3)在容量瓶的使用方法中,下列操作不正确的是BC.
A.使用容量瓶前检查它是否漏水 B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1~2cm处,改用胶头滴管加蒸馏水到标线 D.往容量瓶中转移溶液时应用玻璃棒引流
(4)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是③⑥.
①转移溶液时不慎有少量洒到容量瓶外面
②没有洗涤烧杯和玻璃棒
③定容时俯视刻度线
④容量瓶不干燥,含有少量蒸馏水
⑤定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线.
⑥未冷却到室温就将溶液转移到容量瓶并定容.
分析 (1)配制一定物质的量浓度溶液的步骤:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀,据此选择使用的仪器,然后判断缺少的仪器;
(2)依据C=$\frac{1000ρω}{M}$计算浓硫酸的物质的量浓度,依据溶液稀释过程中溶质的物质的量不变计算需要浓硫酸体积;
(3)根据容量瓶的构造及正确使用容量瓶的方法进行判断;
(4)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)配制一定物质的量浓度溶液的步骤:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀,用到的仪器:量筒、胶头滴管、烧杯、玻璃棒、容量瓶,配制480mL0.92mol•L-1的稀硫酸应选择500mL容量瓶,所以还缺少的仪器:胶头滴管、500ml容量瓶;
故答案为:胶头滴管、500ml容量瓶;
(2)质量分数98%、密度为1.84g•cm-3的浓硫酸,物质的量浓度C=$\frac{1000×1.84×98%}{98}$=18.4mol/L,配制480mL0.92mol•L-1的稀硫酸,应选择500mL容量瓶,实际配制500mL溶液,设需要浓硫酸体积为V,则依据溶液稀释过程中溶质的物质的量不变得:18.4mol/L×V=0.92mol/L×500mL,解得V=25.0mL;
故答案为:25.0;
(3)A.容量瓶是带有活塞的仪器,使用前要检查是否漏水,故A正确;
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗,导致溶质的物质的量偏大,溶液浓度偏高,故B错误;
C.容量瓶为精密仪器,不能用来溶解固体,故C错误;
D.往容量瓶中转移溶液时应用玻璃棒引流,防止液体洒到外面,故D正确;
故选:BC;
(4)①转移溶液时不慎有少量洒到容量瓶外面,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低,故不选;
②没有洗涤烧杯和玻璃棒,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低,故不选;
③定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故选;
④容量瓶不干燥,含有少量蒸馏水,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变,故不选;
⑤定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线,导致溶液体积偏大,溶液浓度偏低,故不选;
⑥未冷却到室温就将溶液转移到容量瓶并定容,冷却后导致溶液体积偏小,溶液浓度偏高,故选;
故答案为:③⑥.
点评 本题主要考查了配制一定物质的量浓度溶液的操作步骤和仪器方法,明确配制原理及容量瓶使用方法是解题关键,题目难度不大,注意误差分析的方法和技巧.

| A. | 分类是学习和研究化学物质及其变化的一种常用方法 | |
| B. | 有些液态胶体也是透明的,用肉眼很难与溶液相区别 | |
| C. | 2 L1 mol/L Na2 CO3溶液中c(Na+)为4 mol/L | |
| D. | 从1 LNaCl溶液中取出100 ml,其浓度与原1L溶液相同 |
| A. | $\frac{m}{23V}$mol/L | B. | $\frac{23}{mV}$mol/L | C. | $\frac{2m}{23V}$mol/L | D. | $\frac{m}{46V}$mol/L |
| A. | 甲烷的标准燃烧热为-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 Mpa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的△H不同 | |
| D. | 101 kPa时,硫的标准燃烧热与硫完全燃烧时的物质的量无关 |
| A. | 离子化合物的熔点一定比共价化合物熔点高 | |
| B. | 甲烷的标准燃烧热为890.3KJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| C. | 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| D. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照条件和点燃条件下的△H相同 |
| A. | 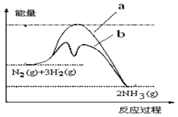 图中曲线b表示工业合成氨中加入铁触媒(催化剂)的能量变化曲线 | |
| B. | 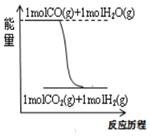 根据图可知在该条件下:CO2(g)+H2(g)═CO(g)+H2O(g)△H<0 | |
| C. |  图中曲线表示向1.0 mol•L-1的醋酸溶液中通入氨气,溶液导电能力的变化情况 | |
| D. |  图中曲线表示常温下向弱酸HA的稀溶液中加水稀释时,c(HA)/c(A-)的变化情况 |