题目内容
15.下列关于氯水的叙述中,正确的是( )| A. | 新制氯水中既有分子,又有离子 | |
| B. | 久置的氯水可以使干燥的有色布条褪色 | |
| C. | 新制氯水中滴加硝酸银溶液,没有任何现象 | |
| D. | 新制氯水在光照条件下,可以产生气体,该气体是氯气 |
分析 A、从新制氯水中的成分来分析;
B、从新制氯水中含有的次氯酸具有漂白性进行分析;
C、从新制氯水中含氯离子,氯离子能和银离子之间反应分析;
D、从新制氯水中含次氯酸不稳定,见光分解为盐酸和氧气.
解答 解:A、新制氯水中存在水分子、次氯酸分子、氯气分子以及氢离子、氯离子、次氯酸根离子、氢氧根离子,故A正确;
B、新制氯水含有次氯酸分子,具有漂白性,可以使干燥的布条褪色,而置的氯水是稀盐酸不能使有色布条褪色,故B错误;
C、新制氯水中含氯离子,滴加硝酸银溶液,会出现白色沉淀,故C错误;
D、新制氯水中存在次氯酸,不稳定,见光分解为盐酸和氧气,不会出现氯气放出,故D错误;
故选A.
点评 本题考查了新制氯水中的成分及各成分的性质,可以根据所学知识来回答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列反应产物属于不饱和烃的是( )
| A. | 苯与氢气的加成反应产物 | B. | 乙醇的消去反应产物 | ||
| C. | 甲烷与氯气的取代反应产物 | D. | 丙烯的加聚反应产物 |
6.阅读表中短周期主族元素的相关信息并填空.
(1)E元素周期表中的位置第2周期、第IVA族;C的原子结构示意图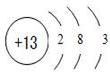 .
.
(2)X的化学式为NaClO.
(3)A、B、D三种元素形成的简单离子半径由大到小的顺序为Cl->O2->Na+(用离子符号表示).
(4)A、B形成的一种原子个数比为1:1化合物的化学式为Na2O2.
(5)A在真空高压下能与由元素D、E组成化合物ED4反应生成两种固体物质,其中一种是自然界中硬度最大的物质,此反应在科学上有“稻草变黄金”的美称.写出该反应的化学方程式4Na+CCl4$\frac{\underline{\;真空高压\;}}{\;}$4NaCl+C.
| 元素代号 | 相关信息 |
| A | A的单质能与冷水剧烈反应,得到强碱性溶液 |
| B | B的原子最外层电子数是其内层电子数的三倍 |
| C | 是地壳中含量最高的金属元素 |
| D | A、B、D组成的化合物X是84消毒剂的主要成分 |
| E | 所有有机物中都含有E元素 |
 .
.(2)X的化学式为NaClO.
(3)A、B、D三种元素形成的简单离子半径由大到小的顺序为Cl->O2->Na+(用离子符号表示).
(4)A、B形成的一种原子个数比为1:1化合物的化学式为Na2O2.
(5)A在真空高压下能与由元素D、E组成化合物ED4反应生成两种固体物质,其中一种是自然界中硬度最大的物质,此反应在科学上有“稻草变黄金”的美称.写出该反应的化学方程式4Na+CCl4$\frac{\underline{\;真空高压\;}}{\;}$4NaCl+C.
10.下列解释过程或事实的方程式不正确的是( )
| A. | Na放入水中,产生气体:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 用催化法处理汽车尾气中的CO和NO:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2 | |
| C. | NaOH溶液不能保存在玻璃塞的试剂瓶中:SiO2+2OH-═SiO32-+H2O | |
| D. | 红热的铁丝与水蒸汽接触,表面形成黑色保护层:2Fe+3H2O(气)$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2 |
4.下列物质中,不能由金属单质直接与盐酸反应制得的是( )
| A. | 氯化铝 | B. | 氯化铁 | C. | 氯化亚铁 | D. | 氯化镁 |
5.下列说法正确的是( )
| A. | 碳酸的酸性比硅酸强 | |
| B. | 136C表示该元素的相对原子质量近似为13,核电荷数为6 | |
| C. | 共价键必然存在于共价化合物中 | |
| D. | X、Y+、Z-三种粒子的电子层结构相同,则其质子数一定不相等 |
 甲醇是一种重要的化工原料,有着重要的用途和应用前景.
甲醇是一种重要的化工原料,有着重要的用途和应用前景.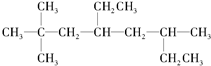 用系统命名法命名烃A2,2,6-三甲基-4-乙基辛烷;烃A的一氯代物具有不同沸点的产物有10种,若烃A由单烯烃与H2加成所得,则原单烯烃有8种结构.
用系统命名法命名烃A2,2,6-三甲基-4-乙基辛烷;烃A的一氯代物具有不同沸点的产物有10种,若烃A由单烯烃与H2加成所得,则原单烯烃有8种结构.