题目内容
5.下列说法正确的是( )| A. | 碳酸的酸性比硅酸强 | |
| B. | 136C表示该元素的相对原子质量近似为13,核电荷数为6 | |
| C. | 共价键必然存在于共价化合物中 | |
| D. | X、Y+、Z-三种粒子的电子层结构相同,则其质子数一定不相等 |
分析 A.同主族从上到下非金属性减弱,非金属性越强,其最高价氧化物的水化物的酸性越强;
B.13C是表示碳原子组成的符号,13为该碳原子的质量数;
C.共价化合物中只含共价键,离子化合物中含有离子键可能含有共价键;
D.原子的电子数等于质子数,离子的电子数与质子数不相等.
解答 解:A.同主族从上到下非金属性减弱,碳与硅同主族,碳元素的非金属性比硅强,故H2CO2酸性强于H2SiO3,故A正确;
B.13C是表示碳原子组成的符号,13为该碳原子的质量数,或者说该碳原子的相对原子质量近似为13,但不是碳元素的相对原子质量,故B错误;
C.共价化合物中只含共价键,离子化合物中含有离子键可能含有共价键,所以共价键不一定存在于共价化合物中,故C错误;
D.X、Y+、Z-三种粒子的电子层结构相同,即电子数相等,阴离子的电子数大于质子数,阳离子的电子数小于质子数,所以其核电荷数或质子数不可能相等,故D正确.
故选AD.
点评 本题考查了元素周期律、共价键等,侧重于基础知识的考查,题目难度不大,注意把握元素周期律的应用.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
15.下列关于氯水的叙述中,正确的是( )
| A. | 新制氯水中既有分子,又有离子 | |
| B. | 久置的氯水可以使干燥的有色布条褪色 | |
| C. | 新制氯水中滴加硝酸银溶液,没有任何现象 | |
| D. | 新制氯水在光照条件下,可以产生气体,该气体是氯气 |
13.为了回收含有Ag+的废水中的贵重金属,可以向其中加入( )
| A. | Fe | B. | 活性炭 | C. | 硫酸亚铁 | D. | 氯化钠 |
20.下列生活中的一些现象发生了化学变化的是 ( )
| A. | 食物发霉 | B. | 冰雪融化 | C. | 铜像生锈 | D. | 聚沙成塔 |
10.下列说法正确的是( )
| A. | 摩尔是国际单位制中七个基本物理量之一 | |
| B. | Cl2的摩尔质量是71 g/mol | |
| C. | 标准状况下,22.4 L H2O的物质的量为1 mol | |
| D. | 1 mol H2的质量是1 g |
17.下列化学用语正确的是( )
| A. | 氯化钠的电子式: | B. | 乙烯的结构式:CHCH | ||
| C. | 磷原子的结构示意图: | D. | 乙酸的分子式:C2H4O2 |
14.某原电池反应原理示意图如图.下列有关该原电池的说法正确的是( )
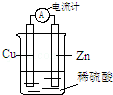

| A. | 将电能转化为化学能 | B. | 一段时间后,铜片质量减轻 | ||
| C. | 电子从锌片经导线流向铜片 | D. | 锌片发生还原反应 |
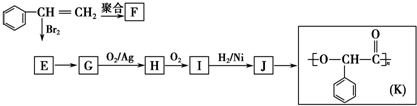
 ;I的结构简式是
;I的结构简式是 .
.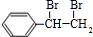 +2NaOH$→_{△}^{水}$
+2NaOH$→_{△}^{水}$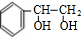 +2NaBr;反应类型属于水解反应.
+2NaBr;反应类型属于水解反应.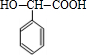 ;反应类型属于加成反应.
;反应类型属于加成反应.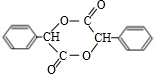 .
.