题目内容
19.下列原子构成的单质中既能与稀硫酸反应又能与烧碱溶液反应,都产生H2的是( )| A. | 核内无中子的原子 | |
| B. | 价电子构型为3s23p1 | |
| C. | 最外层电子数等于倒数第三层上的电子数的原子 | |
| D. | N层上无电子,最外层上的电子数等于电子层数的原子 |
分析 既能与稀硫酸反应又能与烧碱溶液反应,都产生H2,应为Al,原子核外有13个电子,最外层电子数为3,以此解答该题.
解答 解:既能与稀硫酸反应又能与烧碱溶液反应,都产生H2,应为Al,
A.核内无中子的原子为H,故A错误;
B.价电子构型为3s23p1为Al,故B正确;
C.最外层电子数等于倒数第三层上的电子数的原子,为Mg元素,故C错误;
D.N层上无电子,最外层上的电子数等于电子层数的原子,可为H、Be、Al等,故D错误.
故选B.
点评 本题考查原子结构和性质,侧重考查分析推断及发散思维能力,正确判断元素是解本题关键,易错选项是D,熟练掌握物质性质、原子结构、元素周期表结构,题目难度不大.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
10.下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A. | Na2CO3溶液中:2c(Na+)═c(CO32-)+c(HCO3-)+c(H2CO3) | |
| B. | 0.1 mol/L Na2CO3溶液:c(OH-)═c(HCO3-)+c(H+)+2c(H2CO3) | |
| C. | 向醋酸钠溶液中加入一定量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)>c(NO3-) |
14.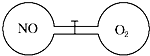 一定温度下,两个体积相等的连通容器用活塞分开,左右两室各充入一定量NO和O2,恰好使两容器内气体密度相同,打开活塞,充分混合反应.下列判断正确的是(不考虑NO2转化为N2O4)( )
一定温度下,两个体积相等的连通容器用活塞分开,左右两室各充入一定量NO和O2,恰好使两容器内气体密度相同,打开活塞,充分混合反应.下列判断正确的是(不考虑NO2转化为N2O4)( )
 一定温度下,两个体积相等的连通容器用活塞分开,左右两室各充入一定量NO和O2,恰好使两容器内气体密度相同,打开活塞,充分混合反应.下列判断正确的是(不考虑NO2转化为N2O4)( )
一定温度下,两个体积相等的连通容器用活塞分开,左右两室各充入一定量NO和O2,恰好使两容器内气体密度相同,打开活塞,充分混合反应.下列判断正确的是(不考虑NO2转化为N2O4)( )| A. | 最终容器内无O2存在 | B. | 反应前、后左室气体压强不变 | ||
| C. | 反应前、后右室气体密度不变 | D. | 开始时左右两室气体分子数相同 |
4.生活中的一些问题常涉及到化学知识,下列叙述正确的是( )
| A. | 明矾[KAl(SO4)2•12H2O]在水中能形成Al(OH)3胶体,可用作消毒剂和净水剂 | |
| B. | 在食品袋中放入盛有硅胶、生石灰的透气小袋,可防止食物受潮 | |
| C. | “雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮氧化物有关 | |
| D. | 食用植物油的重要成分是高级不饱和脂肪酸甘油酯,是天然高分子化合物 |
11.KO2的晶体结构和NaCl相似,KO2可以看作是Na+的位置用K+代替,Cl-的位置用O2-代替,则关于KO2晶体结构的描述正确的是( )
| A. |  如图一个超氧化钾小晶胞中含有4个KO2 | |
| B. | 和K+距离相同且最近的O2-构成的多面体是正六面体 | |
| C. | 和K+距离相同且最近的K+有8个 | |
| D. | 和K+距离相同且最近的O2-共有8个 |
8.将等物质的量的镁和铝相混合,取四份等质量的该混合物分别加到足量的下列溶液中,充分反应后,放出氢气最多的是( )
| A. | 3 mol/L HCl | B. | 4 mol/L HNO3 | C. | 8 mol/L NaOH | D. | 18 mol/L H2SO4 |
9. 向盐酸和AlCl3的混合溶液中逐滴加入NaOH溶液至过量,生成沉淀Al(OH)3的量随着加入NaOH溶液体积的变化关系如图所示,下列说法正确的是
向盐酸和AlCl3的混合溶液中逐滴加入NaOH溶液至过量,生成沉淀Al(OH)3的量随着加入NaOH溶液体积的变化关系如图所示,下列说法正确的是
( )
 向盐酸和AlCl3的混合溶液中逐滴加入NaOH溶液至过量,生成沉淀Al(OH)3的量随着加入NaOH溶液体积的变化关系如图所示,下列说法正确的是
向盐酸和AlCl3的混合溶液中逐滴加入NaOH溶液至过量,生成沉淀Al(OH)3的量随着加入NaOH溶液体积的变化关系如图所示,下列说法正确的是( )
| A. | 在a点对应的溶液中,加入Mg2+、I-、NH4+、NO3-离子仍能大量共存 | |
| B. | 图中B→C的过程中,实际发生的离子方程式为Al(OH)3+OH-=AlO2-+2H2O | |
| C. | 若b、c的纵坐标数值相同,则横坐标数值之比为1:3 | |
| D. | 原溶液中盐酸和AlCl3物质的量的浓度之比为1:3 |
 利用图装置,可以模拟铁的电化学防护.
利用图装置,可以模拟铁的电化学防护. .
.