题目内容
3.W、X、Y、Z均为短周期元素,W-的电子层结构与氦相同,X、Y处在同一周期,X、Y的原子最外层电子数分别为1、6,Z原子的L电子层有7个电子,下列说法正确的是( )| A. | 单质沸点:W>Z | |
| B. | 离子半径:Y2->Z- | |
| C. | 原子序数:Z>Y>X>W | |
| D. | W分别与Y、Z形成的化合物中均只含极性共价键 |
分析 W-的电子层结构与氦相同,则W应为H元素,X、Y处在同一周期,X、Y的原子最外层电子数分别为1、6,X、Y可能为第二或第三周期,X为Li或Na,Y为O或S,Z原子的L电子层有7个电子,为F元素,结合对应单质化合物的性质以及元素周期率的递变规律解答该题.
解答 解:W-的电子层结构与氦相同,则W应为H元素,X、Y处在同一周期,X、Y的原子最外层电子数分别为1、6,X、Y可能为第二或第三周期,X为Li或Na,Y为O或S,Z原子的L电子层有7个电子,为F元素,
A.W为H,Z为F,氟气的相对分子质量较大,分子间作用力较强,沸点较高,故A错误;
B.Z为F,无论Y为O或S,离子半径都大于氟离子,故B正确;
C.因X、Y不能确定,则不能确定原子序数大小,故C错误;
D.H可与O反应生成H2O2,含有非极性键,故D错误.
故选B.
点评 本题考查元素周期率知识,为高频考点,侧重学生的分析能力的考查,注意把握元素结构与性质的关系,把握元素周期率的递变性和相似性,难度中等.

练习册系列答案
相关题目
13.短周期元素的离子:aW3+、bX+、cY2-、dZ-具有相同的电子层结构,下列关系中不正确的是( )
| A. | 半径:Y2->Z->X+>W3+ | B. | 还原性:Y2->Z- | ||
| C. | 氧化性:W3+>X+ | D. | 质子数:c>d>b>a |
14.CH4和CO2可以制造价值更高的化学产品.已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H1=a kJ•mol-1
CO(g)+H2O(g)=CO2(g)+H2(g)△H2=b kJ•mol-1
2CO(g)+O2(g)=2CO2(g)△H3=c kJ•mol-1
则反应CO2(g)+CH4(g)?2CO(g)+2H2(g)的△H用含a、b、c的代数式表示为( )
CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H1=a kJ•mol-1
CO(g)+H2O(g)=CO2(g)+H2(g)△H2=b kJ•mol-1
2CO(g)+O2(g)=2CO2(g)△H3=c kJ•mol-1
则反应CO2(g)+CH4(g)?2CO(g)+2H2(g)的△H用含a、b、c的代数式表示为( )
| A. | a+2b-c | B. | a+b-2c | C. | 2a+2b-c | D. | a+2b-2c |
11.如图是合成一种香料过程的中间产物,下列关于该物质的说法不正确的是( )
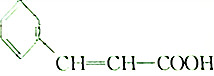
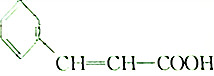
| A. | 该物质能与Na发生反应生成H2 | B. | 该物质能发生加聚反应 | ||
| C. | 该物质在一定件下可发生酯化反应 | D. | 物质的摩尔质量为148 |
18.熟石灰的溶解度随温度变化的曲线如图所示,下列说法正确的是( )
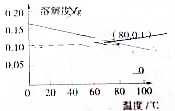

| A. | 熟石灰的溶解是吸热过程 | |
| B. | 温度升高时熟石灰的熔解速率减慢 | |
| C. | 80℃时,熟石灰的Ksp约等于9.8×10-6 | |
| D. | 若硝酸钾中含有少量的熟石灰,可用溶解、过滤的方法进行提纯 |
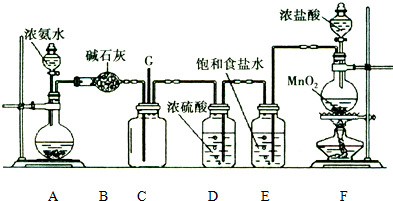
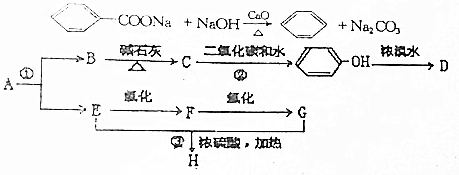
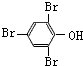 ;化合物H的名称甲酸甲酯.
;化合物H的名称甲酸甲酯.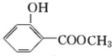 ,
,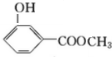 .
.