��Ŀ����
ij�о���ѧϰС��������ͼװ�ý���ͭ��Ũ���ᷴӦ��ʵ���о���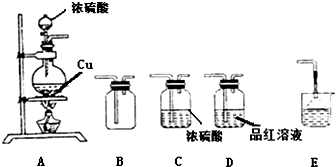
��1��װ��A�з�����Ӧ�Ļ�ѧ����ʽ ��
��2����ҪʹB���ռ��������SO2���壨��֤ʵB�����ռ�������������װ�õ�����˳��Ϊ�� �� �� �� �� ������ĸ��ʾ��
��3������ƿ�г�ַ�Ӧ��ͬѧ�Ƿ���ͭ��ʣ�࣮����ⷢ������Ҳ��ʣ�࣮��ԭ���� ������������ʣ��ķ����� ��
��4���ڲ�����Ũ�����ǰ���£�Ϊʹͭ��һ���ܽ⣬������ƿ�м��� ������ţ�
������ ��FeSO4 ��Fe2O3 ��KNO3��

��1��װ��A�з�����Ӧ�Ļ�ѧ����ʽ
��2����ҪʹB���ռ��������SO2���壨��֤ʵB�����ռ�������������װ�õ�����˳��Ϊ��
��3������ƿ�г�ַ�Ӧ��ͬѧ�Ƿ���ͭ��ʣ�࣮����ⷢ������Ҳ��ʣ�࣮��ԭ����
��4���ڲ�����Ũ�����ǰ���£�Ϊʹͭ��һ���ܽ⣬������ƿ�м���
������ ��FeSO4 ��Fe2O3 ��KNO3��
���㣺Ũ���������ʵ��
ר�⣺
��������1���ڼ��������£�Cu��Ũ���ᷢ��������ԭ��Ӧ����CuSO4��SO2��H2O�����ݷ�Ӧ������P��Ӧ������д����ʽ��
��2����ҪʹB���ռ��������SO2���壨��֤ʵB�����ռ�������װ������˳��Ϊ�����巢��װ�á�����װ�á��ռ�װ�á�����װ�á�β������װ�ã�
��3���ڼ���������Cu��Ũ���ᷢ��������ԭ��Ӧ������ϡ�����Ӧ��ϡ����������ԣ��ܺͽϻ��ý��������û���Ӧ����������
��4��Cu�ڳ������ܺ�Ũ���ᡢϡ���ᷢ�������ᷴӦ���ڲ�����Ũ�����ǰ���£�Ϊʹͭ��һ���ܽ⣬������ƿ�м��뺬����������ӵ����ʻ��ͭ����������ԭ�����ʣ�
��2����ҪʹB���ռ��������SO2���壨��֤ʵB�����ռ�������װ������˳��Ϊ�����巢��װ�á�����װ�á��ռ�װ�á�����װ�á�β������װ�ã�
��3���ڼ���������Cu��Ũ���ᷢ��������ԭ��Ӧ������ϡ�����Ӧ��ϡ����������ԣ��ܺͽϻ��ý��������û���Ӧ����������
��4��Cu�ڳ������ܺ�Ũ���ᡢϡ���ᷢ�������ᷴӦ���ڲ�����Ũ�����ǰ���£�Ϊʹͭ��һ���ܽ⣬������ƿ�м��뺬����������ӵ����ʻ��ͭ����������ԭ�����ʣ�
���
�⣺��1���ڼ��������£�Cu��Ũ���ᷢ��������ԭ��Ӧ����CuSO4��SO2��H2O����Ӧ����ʽΪCu+2H2SO4��Ũ��
CuSO4+SO2��+2H2O���ʴ�Ϊ��Cu+2H2SO4��Ũ��
CuSO4+SO2��+2H2O��
��2����ҪʹB���ռ��������SO2���壨��֤ʵB�����ռ�������װ������˳��Ϊ�����巢��װ�á�����װ�á��ռ�װ�á�����װ�á�β������װ�ã�AΪ���巢��װ�á�BΪ�ռ�װ�á�C�Ǹ���װ�á�D�Ǽ���װ�á�E��β������װ�ã���������˳����ACBDE���ʴ�Ϊ��A��C��B��D��E��
��3���ڼ���������Cu��Ũ���ᷢ��������ԭ��Ӧ������ϡ�����Ӧ�����ŷ�Ӧ�Ľ��У������Ũ�Ȼ��ϡ��ͭ���������ᷴӦ������ͭ�����ᶼ��ʣ�ࣻ
ϡ����������ԣ��ܺͽϻ��ý��������û���Ӧ�������������Լ���������ʣ��ķ�����ȡ��Ӧ�����Һ������пƬ���������ݲ�������˵��������ʣ�࣬
�ʴ�Ϊ�����ŷ�Ӧ�Ľ��У������Ũ�Ȼ��ϡ��ͭ���������ᷴӦ������ͭ�����ᶼ��ʣ�ࣻȡ��Ӧ�����Һ������пƬ���������ݲ�������˵��������ʣ�ࣻ
��4��Cu�ڳ������ܺ�Ũ���ᡢϡ���ᷢ�������ᷴӦ���ڲ�����Ũ�����ǰ���£�Ϊʹͭ��һ���ܽ⣬������ƿ�м��뺬����������ӵ����ʻ���ͭ����������ԭ��Ӧ�����ʣ�
����������������ԣ���ͭ����Ӧ���ʴ���
��Fe�Ļ�ԭ�Դ���Cu������ͭ��FeSO4����Ӧ���ʴ���
��Fe2O3��ϡ���ᷴӦ��������������������Cu����������ԭ��Ӧ���ܽ�Cu������ȷ��
�����������£���������Ӿ���ǿ�����ԣ�������Cu����ͭ�Σ����Լ���KNO3�����ܽ�Cu������ȷ��
�ʴ�Ϊ���ۢܣ�
| ||
| ||
��2����ҪʹB���ռ��������SO2���壨��֤ʵB�����ռ�������װ������˳��Ϊ�����巢��װ�á�����װ�á��ռ�װ�á�����װ�á�β������װ�ã�AΪ���巢��װ�á�BΪ�ռ�װ�á�C�Ǹ���װ�á�D�Ǽ���װ�á�E��β������װ�ã���������˳����ACBDE���ʴ�Ϊ��A��C��B��D��E��
��3���ڼ���������Cu��Ũ���ᷢ��������ԭ��Ӧ������ϡ�����Ӧ�����ŷ�Ӧ�Ľ��У������Ũ�Ȼ��ϡ��ͭ���������ᷴӦ������ͭ�����ᶼ��ʣ�ࣻ
ϡ����������ԣ��ܺͽϻ��ý��������û���Ӧ�������������Լ���������ʣ��ķ�����ȡ��Ӧ�����Һ������пƬ���������ݲ�������˵��������ʣ�࣬
�ʴ�Ϊ�����ŷ�Ӧ�Ľ��У������Ũ�Ȼ��ϡ��ͭ���������ᷴӦ������ͭ�����ᶼ��ʣ�ࣻȡ��Ӧ�����Һ������пƬ���������ݲ�������˵��������ʣ�ࣻ
��4��Cu�ڳ������ܺ�Ũ���ᡢϡ���ᷢ�������ᷴӦ���ڲ�����Ũ�����ǰ���£�Ϊʹͭ��һ���ܽ⣬������ƿ�м��뺬����������ӵ����ʻ���ͭ����������ԭ��Ӧ�����ʣ�
����������������ԣ���ͭ����Ӧ���ʴ���
��Fe�Ļ�ԭ�Դ���Cu������ͭ��FeSO4����Ӧ���ʴ���
��Fe2O3��ϡ���ᷴӦ��������������������Cu����������ԭ��Ӧ���ܽ�Cu������ȷ��
�����������£���������Ӿ���ǿ�����ԣ�������Cu����ͭ�Σ����Լ���KNO3�����ܽ�Cu������ȷ��
�ʴ�Ϊ���ۢܣ�
������������ͭ��Ũ����ķ�ӦΪ���忼��Ũ���ᡢͭ�����ʣ����ؿ���ѧ��ʵ����������������������ʵ��Ŀ������װ��˳���״�ѡ���ǣ�4����ע��������������������ӵ����ʣ���Ŀ�ѶȲ���

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
�����и�����������Һ�У�һ���ܴ���������������ǣ�������
| A����ˮ�����c��H+��=l��l0-14mol/L����Һ�У�Ca2+��K+��Cl-��HCO3- |
| B����ʹpH��ֽ�ʺ�ɫ����Һ��Na+��NH4+��I-��NO3- |
| C��Kw/c��H+��=0.1mol/L����Һ��Na+��K+��SiO32-��NO3- |
| D��FeCl2��Һ��K+��Na+��SO42-��AlO2- |
ˮ��ҺX��ֻ��������K+��Ca2+��A102-��SiO32-��CO32-��SO42-�е����������ӣ�ijͬѧ�Ը����н���������ʵ�������ж���ȷ���ǣ�������


| A�������Ħ������Ϊ44 |
| B���������ǹ������ƵĻ���� |
| C��K+��CO32-��A102-��SiO32-һ����������ҺX�� |
| D��SO42-һ������������ҺX�� |


 +H2O��R1��R2��R3Ϊ��������ԭ�ӣ�
+H2O��R1��R2��R3Ϊ��������ԭ�ӣ� �к��з��ǻ����õ��Լ���
�к��з��ǻ����õ��Լ���
 Na2O2��ˮ�ķ�Ӧʵ�ʿ��Էֽ�Ϊ�����Σ�Na2O2+2H2O=2NaOH+H2O2����Ӧ���ȣ���Ӧ�ų�������ʹ����H2O2���ȷֽ⣺2H2O2=2H2O+O2����Ϊ�˲ⶨij�������ƹ���Ĵ��ȣ���������ʵ�飺
Na2O2��ˮ�ķ�Ӧʵ�ʿ��Էֽ�Ϊ�����Σ�Na2O2+2H2O=2NaOH+H2O2����Ӧ���ȣ���Ӧ�ų�������ʹ����H2O2���ȷֽ⣺2H2O2=2H2O+O2����Ϊ�˲ⶨij�������ƹ���Ĵ��ȣ���������ʵ�飺