题目内容
在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A、由水电离的c(H+)=l×l0-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| B、能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- |
| C、Kw/c(H+)=0.1mol/L的溶液:Na+、K+、SiO32-、NO3- |
| D、FeCl2溶液:K+、Na+、SO42-、AlO2- |
考点:离子共存问题
专题:
分析:A.由水电离的c(H+)=l×l0-14mol/L的溶液中存在大量氢离子或氢氧根离子,碳酸氢根能够与氢离子、氢氧根离子反应;
B.能使pH试纸呈红色的溶液为酸性溶液,溶液中存在大量氢离子,硝酸根离子在酸性条件下能够氧化碘离子;
C.该溶液中氢氧根离子浓度为0.1mol/L,Na+、K+、SiO32-、NO3-之间不发生反应,都不与氢氧根离子反应;
D.亚铁离子与偏铝酸根离子发生双水解反应.
B.能使pH试纸呈红色的溶液为酸性溶液,溶液中存在大量氢离子,硝酸根离子在酸性条件下能够氧化碘离子;
C.该溶液中氢氧根离子浓度为0.1mol/L,Na+、K+、SiO32-、NO3-之间不发生反应,都不与氢氧根离子反应;
D.亚铁离子与偏铝酸根离子发生双水解反应.
解答:
解:A.该溶液为酸性或碱性溶液,碱性溶液中,Ca2+、HCO3-与氢氧根离子发生反应生成碳酸钙沉淀,酸性溶液中,HCO3-与氢离子反应,在溶液中不能大量共存,故A错误;
B.能使pH试纸呈红色的溶液中存在大量氢离子,I-、NO3-之间在酸性条件下能够发生氧化还原反应,在溶液中不能大量共存,故B错误;
C.该溶液为为碱性溶液,溶液中存在大量氢氧根离子,Na+、K+、SiO32-、NO3-之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故C正确;
D.AlO2-与发生双水解反应生成氢氧化亚铁和氢氧化铝沉淀,在溶液中不能大量共存,故D错误;
故选C.
B.能使pH试纸呈红色的溶液中存在大量氢离子,I-、NO3-之间在酸性条件下能够发生氧化还原反应,在溶液中不能大量共存,故B错误;
C.该溶液为为碱性溶液,溶液中存在大量氢氧根离子,Na+、K+、SiO32-、NO3-之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故C正确;
D.AlO2-与发生双水解反应生成氢氧化亚铁和氢氧化铝沉淀,在溶液中不能大量共存,故D错误;
故选C.
点评:本题考查离子共存的正误判断,为中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
在容积相等的两个密闭容器A和B中,保持温度为423K,同时向A、B中分别加入a mol和b mol HI(a>b),发生反应2HI(g)?H2(g)+I2(g)达到平衡后,下列说法中,正确的是( )
| A、从开始反应到达平衡,所需时间tA>tB |
| B、平衡时,I2蒸气在混合气体中的体积分数φA>φB |
| C、平衡时,I2蒸气的物质的量浓度[I2]A=[I2]B |
| D、HI的平衡转化率,αA=αB |
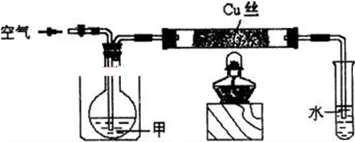
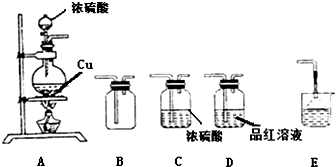
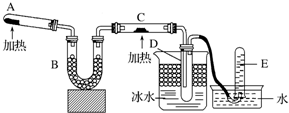 已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应.
已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应.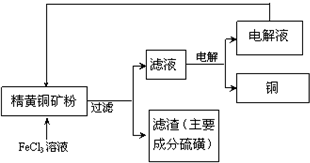 工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜,有如下两种工艺.
工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜,有如下两种工艺.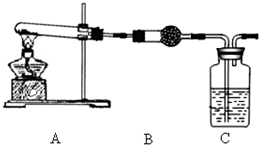
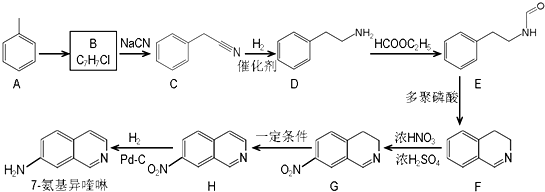
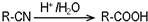 .请回答下列问题:
.请回答下列问题: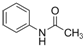 ),请设计合成路线(无机试剂及溶剂任选).
),请设计合成路线(无机试剂及溶剂任选).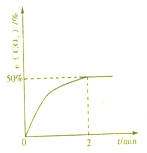 处理含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S(g).发生反应为:2CO(g)+SO2(g)?S(g)+2CO2(g)
处理含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S(g).发生反应为:2CO(g)+SO2(g)?S(g)+2CO2(g)