题目内容
16.某元素原子的原子核外有三个电子层,最外层电子数是4,该原子的原子序数是( )| A. | 14 | B. | 15 | C. | 16 | D. | 17 |
分析 元素原子的原子核外有三个电子层,最外层有4个电子,由电子排布规律可知原子的电子数,电子数=质子数.
解答 解:因元素原子的原子核外有三个电子层,最外层有4个电子,
第一层电子数只能为2,
第二层电子数只能为8,
第三层(最外层)电子数为4,
则原子核外电子数为2+8+4=14,
所以质子数为14,
故选A.
点评 本题考查原子的结构和原子的质子数,明确电子排布规律即可解答,难度不大.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
7.在C5H11Cl的同分异构体中,若其结构中只含有两个-CH3,则该物质的结构(不考虑顺反异构)最多有( )
| A. | 6种 | B. | 7种 | C. | 5种 | D. | 4种 |
4.某元素的一种同位素X的原子质量数为A,含N个中子,它与11H原子组成HmX分子.在a 克HmX中所含质子的物质的量是( )
| A. | $\frac{a}{m+A}$(A-N+m)mol | B. | $\frac{a}{A}$(A一N)mol | C. | $\frac{a}{m+A}$(A-N)mol | D. | $\frac{a}{A}$(A一N+m)mol |
11.对于在密闭容器中进行的可逆反应2SO2(g)+18O2(g)?2SO3(g),下列说法正确的是( )
| A. | 容器内只含有18O2、SO2、SO3三种分子 | |
| B. | 18O只存在18O2分子中 | |
| C. | 容器内含有18O2、S18O2、S18O3等分子 | |
| D. | 反应达到限度时,所有物质的质量都相等 |
1.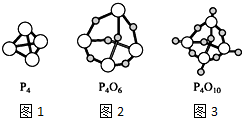 如图,图1表示白磷(P4)的分子结构,图2表示三氧化二磷(P4O6)的分子结构,图3表示五氧化二磷(P4O10)的分子结构,下列说法中正确的是( )
如图,图1表示白磷(P4)的分子结构,图2表示三氧化二磷(P4O6)的分子结构,图3表示五氧化二磷(P4O10)的分子结构,下列说法中正确的是( )
 如图,图1表示白磷(P4)的分子结构,图2表示三氧化二磷(P4O6)的分子结构,图3表示五氧化二磷(P4O10)的分子结构,下列说法中正确的是( )
如图,图1表示白磷(P4)的分子结构,图2表示三氧化二磷(P4O6)的分子结构,图3表示五氧化二磷(P4O10)的分子结构,下列说法中正确的是( )| A. | P4O6中的磷原子采用sp2方式杂化 | |
| B. | 三氧化二磷、五氧化二磷这两个名称都表示分子的实际组成 | |
| C. | P4、P4O6和P4O10分子中同一P原子上两个化学键之间的夹角都是60° | |
| D. | P4O6分子中4个P原子构成正四面体,6个O原子构成正八面体 |
8.下列离子中外层d轨道完全充满状态的是( )
| A. | Cr3+ | B. | Fe3+ | C. | CO3+ | D. | Cu+ |
5.元素周期表揭示了化学元素间的内在联系,有关元素周期表的说法不正确的是( )
| A. | 俄国化学家门捷列夫编制了第一张元素周期表 | |
| B. | 周期表中最外层电子数相同的元素都排列在同一列中 | |
| C. | 周期表中一共有18列,但只有16个族 | |
| D. | 随着人们的认识的发展,周期表也在不断的发展变化着 |
6.下列叙述正确的是( )
| A. | 所有卤代烃都难溶于水,且都是密度比水大的液体 | |
| B. | 所有卤代烃都是通过取代反应制得,且都是良好的有机溶剂 | |
| C. | 煮沸氯乙烷和氢氧化钠的醇溶液能发生消去反应 | |
| D. | 煮沸氯乙烷和氢氧化钠溶液能发生加成反应 |



