题目内容
聚合氯化铝是一种新型净水剂,其中铝的总浓度(用AlT表示)包括三类‘“主要为Al3+的单体形态铝总浓度(用Ala表示);主要为[AlO4Al12(OH)24(H2O)12]7+的中等聚合形态铝总浓度(用Alb表示)和Al(OH)3胶体形态铝总浓度(用A1c表示).
(1)一定条件下,向1.0mo!?L-1 AlCl3溶液中加入0.6mol?L-1的NaOH溶液,可制得Alb含量约为86%的聚合氯化铝溶液.写出生成[AlO4Al12(OH)24(H2O)12]7+的离子方程式:
(2)用膜蒸馏(简称MD)浓缩技术将聚合氯化铝溶液进行浓缩,实验过程中不同浓度聚合氯化铝中铝形态分布(百分数)如下表:
①在一定温度下,AlT越大.pH (填“越大”、“越小”或“不变”).
②如将AlT=2.520mol?L-1的聚合氯化铝溶液加水稀释,则稀释过程中主要发生反应的离子方程式: .
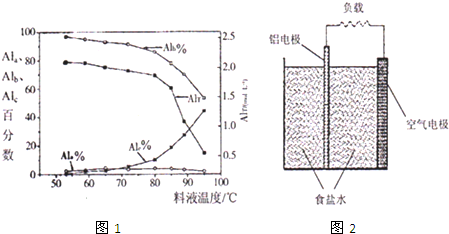
③膜蒸馏料液温度对铝聚合形态百分数及铝的总浓度的影响如图1.当T>80℃时,AlT显著下降的原因是 .
(3)真空碳热还原一氧化法可实现由铝土矿制备金属铝,相关反应的热化学方程式如下:
①Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g)△H1=a kJ?mol-1
②3AlCl(g)=2Al(l)+AlCl3(g)△H2=b kJ?mol-1
则反应Al2O3(s)+3C(s)=2Al(l)++3CO(g)△H= kJ?mol-1(用含a、b的代数式表示).反应①常压下在1900℃的高温下才能进行,说明△H 0(填“>”“=”或“<”).
(4)一种铝空气电池结构如图2所示,写出该电池正极的电极反应式 .
(1)一定条件下,向1.0mo!?L-1 AlCl3溶液中加入0.6mol?L-1的NaOH溶液,可制得Alb含量约为86%的聚合氯化铝溶液.写出生成[AlO4Al12(OH)24(H2O)12]7+的离子方程式:
(2)用膜蒸馏(简称MD)浓缩技术将聚合氯化铝溶液进行浓缩,实验过程中不同浓度聚合氯化铝中铝形态分布(百分数)如下表:
| AlT/(mol?L-1) | Ala/% | Alb/% | A1c/% |
| 0.208 | 1.4 | 86.6 | 12.0 |
| 0.489 | 2.3 | 86.2 | 11.5 |
| 0.884 | 2.3 | 88.1 | 9.6 |
| 1.613 | 3.1 | 87.0 | 9.9 |
| 2.520 | 4.5 | 88.2 | 7.3 |
②如将AlT=2.520mol?L-1的聚合氯化铝溶液加水稀释,则稀释过程中主要发生反应的离子方程式:
③膜蒸馏料液温度对铝聚合形态百分数及铝的总浓度的影响如图1.当T>80℃时,AlT显著下降的原因是

(3)真空碳热还原一氧化法可实现由铝土矿制备金属铝,相关反应的热化学方程式如下:
①Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g)△H1=a kJ?mol-1
②3AlCl(g)=2Al(l)+AlCl3(g)△H2=b kJ?mol-1
则反应Al2O3(s)+3C(s)=2Al(l)++3CO(g)△H=
(4)一种铝空气电池结构如图2所示,写出该电池正极的电极反应式
考点:用盖斯定律进行有关反应热的计算,电极反应和电池反应方程式,镁、铝的重要化合物
专题:化学反应中的能量变化,电化学专题
分析:(1)根据题意结合原子守恒、电荷守恒可得生成[AlO4Al12(OH)24(H2O)12]7+,的离子方程式;
(2)①在一定温度下,AlT越大,Ala%越大,Alc%越小,所以pH减小;
②如将AlT=2.520mol?L-1的聚合氯化铝溶液加水稀释,则稀释过程中主要发生反应的离子方程式:Al3++3H2O?Al(OH)3(胶体)+3H+;
③膜蒸馏料液温度对铝聚合形态百分数及铝的总浓度的影响如图所示,当T>80℃时,AlT显著下降的原因是温度升高,水解程度加大,产生氢氧化铝沉淀;
(3)由盖斯定律可知:①+②得Al2O3(s)+3C(s)=2Al(l)+3CO(g)△H;反应①常压下在1900℃的高温下才能进行,说明该反应是吸热反应,△H>0;
(4)在该铝空气电池中活动性强的Al作负极,活动性弱的C作正极.由于是在中性介质中,所以发生的是吸氧腐蚀.
(2)①在一定温度下,AlT越大,Ala%越大,Alc%越小,所以pH减小;
②如将AlT=2.520mol?L-1的聚合氯化铝溶液加水稀释,则稀释过程中主要发生反应的离子方程式:Al3++3H2O?Al(OH)3(胶体)+3H+;
③膜蒸馏料液温度对铝聚合形态百分数及铝的总浓度的影响如图所示,当T>80℃时,AlT显著下降的原因是温度升高,水解程度加大,产生氢氧化铝沉淀;
(3)由盖斯定律可知:①+②得Al2O3(s)+3C(s)=2Al(l)+3CO(g)△H;反应①常压下在1900℃的高温下才能进行,说明该反应是吸热反应,△H>0;
(4)在该铝空气电池中活动性强的Al作负极,活动性弱的C作正极.由于是在中性介质中,所以发生的是吸氧腐蚀.
解答:
解:(1)向1.0mo!?L-1 AlCl3溶液中加入0.6mol?L-1的NaOH溶液,可制得Alb含量约为86%的聚合氯化铝溶液,根据题意结合原子守恒、电荷守恒可得生成[AlO4Al12(OH)24(H2O)12]7+,的离子方程式为13Al3++32OH-+8H2O=[AlO4Al12(OH)24(H2O)12]7+,
故答案为:13Al3++32OH-+8H2O=[AlO4Al12(OH)24(H2O)12]7+;
(2)①在一定温度下,AlT越大,Ala%越大,Alc%越小,所以pH减小,故答案为:减小;
②如将AlT=2.520mol?L-1的聚合氯化铝溶液加水稀释,则稀释过程中主要发生反应的离子方程式:Al3++3H2O?Al(OH)3(胶体)+3H+,
故答案为:Al3++3H2O?Al(OH)3(胶体)+3H+;
③膜蒸馏料液温度对铝聚合形态百分数及铝的总浓度的影响如图所示,当T>80℃时,AlT显著下降的原因是温度升高,水解程度加大,产生氢氧化铝沉淀,
故答案为:温度升高,水解程度加大,产生氢氧化铝沉淀;
(3)①Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g)△H1=a kJ?mol-1
②3AlCl(g)=2Al(l)+AlCl3(g)△H2=b kJ?mol-1
由盖斯定律可知①+②可得Al2O3(s)+3C(s)=2Al(l)+3CO(g)△H=△H1+△H2=(a+b)kJ/mol,
反应①常压下在1900℃的高温下才能进行,说明该反应是吸热反应,△H>0,
故答案为:a+b;>;
(4)在该铝空气电池中活动性强的Al作负极,活动性弱的C作正极.由于是在中性介质中,所以发生的是吸氧腐蚀.该电池正极的电极反应式是O2+2H2O+4e-=4OH-,
故答案为:O2+2H2O+4e-=4OH-.
故答案为:13Al3++32OH-+8H2O=[AlO4Al12(OH)24(H2O)12]7+;
(2)①在一定温度下,AlT越大,Ala%越大,Alc%越小,所以pH减小,故答案为:减小;
②如将AlT=2.520mol?L-1的聚合氯化铝溶液加水稀释,则稀释过程中主要发生反应的离子方程式:Al3++3H2O?Al(OH)3(胶体)+3H+,
故答案为:Al3++3H2O?Al(OH)3(胶体)+3H+;
③膜蒸馏料液温度对铝聚合形态百分数及铝的总浓度的影响如图所示,当T>80℃时,AlT显著下降的原因是温度升高,水解程度加大,产生氢氧化铝沉淀,
故答案为:温度升高,水解程度加大,产生氢氧化铝沉淀;
(3)①Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g)△H1=a kJ?mol-1
②3AlCl(g)=2Al(l)+AlCl3(g)△H2=b kJ?mol-1
由盖斯定律可知①+②可得Al2O3(s)+3C(s)=2Al(l)+3CO(g)△H=△H1+△H2=(a+b)kJ/mol,
反应①常压下在1900℃的高温下才能进行,说明该反应是吸热反应,△H>0,
故答案为:a+b;>;
(4)在该铝空气电池中活动性强的Al作负极,活动性弱的C作正极.由于是在中性介质中,所以发生的是吸氧腐蚀.该电池正极的电极反应式是O2+2H2O+4e-=4OH-,
故答案为:O2+2H2O+4e-=4OH-.
点评:本题考查了物质的存在形式与溶液酸碱性的关系、离子方程式的书写、反应的热效应的判断、原电池反应原理的知识,综合性非常强,难度较大,很好的体现了学生对化学反应原理的掌握程度.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
向含有0.010mol?L-1 CrO42-离子和0.010mol?L-1 SO42-离子的混合溶液中,逐滴加入少量Pb(NO3)2溶液(忽略加入Pb(NO3)2所引起的体积变化),下列说法正确的是(KSP (PbCrO4)=2.8×10-13,KSP (PbSO4)=2.8×10-8)( )
| A、PbCrO4先沉淀 |
| B、PbSO4先沉淀 |
| C、PbCrO4和PbSO4一起沉淀 |
| D、PbCrO4和PbSO4都不沉淀 |
某温度下将2mol A和3mol B充入一密闭容器中发生反应:aA(g)+B(g)?C(g)+D(g),5min后达到平衡,已知各物质的平衡浓度关系有C(A)?C(B)=C(C)?C(D),若在温度不变的情况下将容器体积扩大为原来的10倍时,A的转化率不发生变化,则B的转化率为( )
| A、60% | B、24% |
| C、30% | D、40% |
下列区别物质的方法错误的是( )
| A、用肥皂水区别软水和硬水 |
| B、用带火星的木条鉴别氧气和空气 |
| C、用燃烧的方法区别羊毛和涤纶 |
| D、用观察颜色的方法区别O2和CO2 |
下列说法正确的是( )
| A、水是人体的重要组成成分,是人体中含量最多的一种物质 |
| B、淀粉在体内必须转换为葡萄糖才能被机体利用,而这种转换不需水参加 |
| C、水约占人体体重的三分之一,由于水分不断代谢,故人体内的水分需不断补充 |
| D、喝纯净水比喝矿泉水更有利于人体健康 |
