题目内容
要检验淀粉的水解程度,提供了以下实验操作过程:①取少量淀粉加水制成溶液 ②加热(水溶)③加入碱液,中和并呈碱性 ④加入银氨溶液 ⑤加入几滴稀硫酸 ⑥再加热 ⑦加入几滴碘水
请指出要达到下列实验目的所需正确操作过程的排列顺序:
(1)证明淀粉尚未水解 ;
(2)证明淀粉正在水解 ;
(3)证明淀粉已完全水解 .
请指出要达到下列实验目的所需正确操作过程的排列顺序:
(1)证明淀粉尚未水解
(2)证明淀粉正在水解
(3)证明淀粉已完全水解
考点:物质的检验和鉴别的实验方案设计
专题:
分析:(1)尚未水解只需证明不存在能发生银镜反应的葡萄糖即可.
(2)正在水解需证明产生了能发生银镜反应的葡萄糖,又有能遇碘单质变蓝的淀粉.
(3)已完全水解只需证明不再有淀粉即可.
(2)正在水解需证明产生了能发生银镜反应的葡萄糖,又有能遇碘单质变蓝的淀粉.
(3)已完全水解只需证明不再有淀粉即可.
解答:
解:(1)证明淀粉尚未水解,则操作为①取少量淀粉加水制成溶液、⑤加入几滴稀硫酸、②加热(水溶)、③加入碱液,中和并呈碱性、④加入银氨溶液、⑥再加热,不生成银镜,故答案为:①⑤②③④⑥;
(2)证明淀粉正在水解,则操作为①取少量淀粉加水制成溶液、⑤加入几滴稀硫酸、②加热(水溶)、③加入碱液,中和并呈碱性、④加入银氨溶液、⑥再加热,生成银镜,说明发生水解,然后①取少量淀粉加水制成溶液、⑤加入几滴稀硫酸、②加热(水溶)、⑦加入几滴碘水,溶液变蓝,则水解正在进行,还有淀粉剩余,
故答案为:①⑤②③④⑥,①⑤②⑦;
(3)证明淀粉完全水解,则操作为①取少量淀粉加水制成溶液、⑤加入几滴稀硫酸、②加热(水溶)、⑦加入几滴碘水,溶液不变蓝,说明水解完全,溶液中不存在淀粉,故答案为:①⑤②⑦.
(2)证明淀粉正在水解,则操作为①取少量淀粉加水制成溶液、⑤加入几滴稀硫酸、②加热(水溶)、③加入碱液,中和并呈碱性、④加入银氨溶液、⑥再加热,生成银镜,说明发生水解,然后①取少量淀粉加水制成溶液、⑤加入几滴稀硫酸、②加热(水溶)、⑦加入几滴碘水,溶液变蓝,则水解正在进行,还有淀粉剩余,
故答案为:①⑤②③④⑥,①⑤②⑦;
(3)证明淀粉完全水解,则操作为①取少量淀粉加水制成溶液、⑤加入几滴稀硫酸、②加热(水溶)、⑦加入几滴碘水,溶液不变蓝,说明水解完全,溶液中不存在淀粉,故答案为:①⑤②⑦.
点评:本题考查淀粉水解实验的设计,为高频考点,把握淀粉的性质及水解生成葡萄糖的性质为解答的关键,侧重性质应用的考查,注意实验设计与物质性质的关系,题目难度不大.

练习册系列答案
相关题目
下列关于不溶物之间转化的说法中错误的是(已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16)( )
A、常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于
| ||||
| B、两种不溶物的Ksp相差越大,不溶物就越容易转化为更难溶的不溶物 | ||||
| C、AgI比AgCl更难溶于水,所以AgCl可以转化为AgI | ||||
| D、AgCl不溶于水,不能转化为AgI |
某一反应在一定条件下的平衡转化率为25.3%,当使用了催化剂时,其转化率为( )
| A、大于25.3% |
| B、小于25.3% |
| C、等于25.3% |
| D、约等于25.3% |
下列各组稀溶液,不用其他试剂,就可以将它们区分开的是( )
| A、氯化铁、氯化钡、碳酸钠、硫酸 |
| B、盐酸、硝酸铵、氢氧化钠、硝酸钠 |
| C、氢氧化钠、稀硫酸、碳酸钠、硫酸氢钠 |
| D、氯化钡、硫酸钠、氯化钙、硝酸钙 |
某有机物A是农药生产中的一种中间体,其结构简式如图所示,下列叙述正确的是( )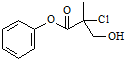

| A、有机物A属于芳香烃 |
| B、有机物A可以和Br2的CCl4溶液发生加成反应 |
| C、有机物A遇FeCl3溶液显紫色 |
| D、1molA和足量的NaOH溶液反应,最多可以消耗3molNaOH |
甲烷燃烧反应的反应类型属于( )
| A、取代反应 | B、加成反应 |
| C、氧化反应 | D、还原反应 |
蔬菜具有一定的调节新陈代谢、维持身体健康的功能,其主要原因是蔬菜富含人体需要的( )
| A、维生素 | B、油脂 |
| C、淀粉 | D、蛋白质 |
 碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是理想,更是一种值得期待的新的生活方式,请运用化学反应原理的相关知识研究碳及其化合物的性质.
碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是理想,更是一种值得期待的新的生活方式,请运用化学反应原理的相关知识研究碳及其化合物的性质.