题目内容
 【化学--选修5有机化学基础】
【化学--选修5有机化学基础】带有支链的某烃A的分子式为C6H14,若烃A的一氯取代物只有3种,分别是B、C、D,且有如图的转化.请回答下列问题:
(1)C的名称为
(2)0.1mol该烃A完全燃烧的产物被碱石灰完全吸收,碱石灰的质量增加
(3)写出下列反应的类型:②
(4)写出D→E的化学方程式
(5)H的同分异构体中符合下列条件的共有
①属于酯类化合物;②水解产物含有相同数目的碳原子.
考点:有机物的推断
专题:有机物的化学性质及推断
分析:C6H14为己烷,A只有三种一氯取代产物:B、C和D,说明A分子中含有三种等效H原子,则A的结构简式为:(CH3)3CCH2CH3;
B和D分别与强碱的醇溶液共热发生消去反应都能得到有机化合物E,则E为:(CH3)3CCH=CH2;B在氢氧化钠的水溶液中发生取代反应生成F、F能发生催化氧化生成G、G被氧化生成H,且F与H在浓硫酸作用下加热反应生成I,则I为酯、F为醇、H为羧酸,则B为(CH3)3CCH2CH2Cl、F为(CH3)3CCH2CH2OH、G为(CH3)3CCH2CHO、H为(CH3)3CCH2COOH、D为(CH3)3CCH2ClCH3)、C为CH2Cl(CH3)2CCH2CH3,I为(CH3)3CCH2COOCH2CH2C(CH3)3,据此进行解答.
B和D分别与强碱的醇溶液共热发生消去反应都能得到有机化合物E,则E为:(CH3)3CCH=CH2;B在氢氧化钠的水溶液中发生取代反应生成F、F能发生催化氧化生成G、G被氧化生成H,且F与H在浓硫酸作用下加热反应生成I,则I为酯、F为醇、H为羧酸,则B为(CH3)3CCH2CH2Cl、F为(CH3)3CCH2CH2OH、G为(CH3)3CCH2CHO、H为(CH3)3CCH2COOH、D为(CH3)3CCH2ClCH3)、C为CH2Cl(CH3)2CCH2CH3,I为(CH3)3CCH2COOCH2CH2C(CH3)3,据此进行解答.
解答:
解:C6H14为己烷,A只有三种一氯取代产物:B、C和D,说明A分子中含有三种等效H原子,则A的结构简式为:(CH3)3CCH2CH3;
B和D分别与强碱的醇溶液共热发生消去反应都能得到有机化合物E,则E为:(CH3)3CCH=CH2;B在氢氧化钠的水溶液中发生取代反应生成F、F能发生催化氧化生成G、G被氧化生成H,且F与H在浓硫酸作用下加热反应生成I,则I为酯、F为醇、H为羧酸,则B为(CH3)3CCH2CH2Cl、F为(CH3)3CCH2CH2OH、G为(CH3)3CCH2CHO、H为(CH3)3CCH2COOH、D为(CH3)3CCH2ClCH3)、C为CH2Cl(CH3)2CCH2CH3,I为(CH3)3CCH2COOCH2CH2C(CH3)3,
(1)根据分析可知,C的结构简式为:CH2Cl(CH3)2CCH2CH3,其名称为:2,2-二甲基-1-氯丁烷;G的结构简式为:(CH3)3CCH2CHO,其含有的官能团为醛基,
故答案为:2,2-二甲基-1-氯丁烷;醛基;
(2)烃A的分子式为C6H14,根据质量守恒定律,0.1molA完全燃烧生成0.6mol二氧化碳、0.7mol水,碱石灰增重的质量为二氧化碳和水的质量,则碱石灰增重的质量为:44g/mol×0.6mol+18g/mol×0.7mol=39g,
故答案为:39 g;
(3)反应②F与H发生酯化反应生成I:(CH3)3CCH2COOCH2CH2C(CH3)3,该反应也属于取代反应;反应③为醇的消去反应,
故答案为:取代反应;消去反应;
(4)D为(CH3)3CCH2ClCH3)、E为(CH3)3CCH=CH2,D→E为卤代烃的消去反应,其反应的化学方程式为:(CH3)3CCHClCH3+NaOH
(CH3)3CCH=CH2+NaCl+H2O,
故答案为:(CH3)3CCHClCH3+NaOH
(CH3)3CCH=CH2+NaCl+H2O;
(5)H为(CH3)3CCH2COOH,H的同分异构体中符合下列条件:①属于酯类化合物,分子中含有官能团酯基;②水解产物含有相同数目的碳原子,生成该酯的醇和羧酸具有相同的C原子,满足条件的酯有:CH3CH2COOCH2CH2CH3、CH3CH2COOCH(CH3)CH3,总共有两种,
故答案为:2.
B和D分别与强碱的醇溶液共热发生消去反应都能得到有机化合物E,则E为:(CH3)3CCH=CH2;B在氢氧化钠的水溶液中发生取代反应生成F、F能发生催化氧化生成G、G被氧化生成H,且F与H在浓硫酸作用下加热反应生成I,则I为酯、F为醇、H为羧酸,则B为(CH3)3CCH2CH2Cl、F为(CH3)3CCH2CH2OH、G为(CH3)3CCH2CHO、H为(CH3)3CCH2COOH、D为(CH3)3CCH2ClCH3)、C为CH2Cl(CH3)2CCH2CH3,I为(CH3)3CCH2COOCH2CH2C(CH3)3,
(1)根据分析可知,C的结构简式为:CH2Cl(CH3)2CCH2CH3,其名称为:2,2-二甲基-1-氯丁烷;G的结构简式为:(CH3)3CCH2CHO,其含有的官能团为醛基,
故答案为:2,2-二甲基-1-氯丁烷;醛基;
(2)烃A的分子式为C6H14,根据质量守恒定律,0.1molA完全燃烧生成0.6mol二氧化碳、0.7mol水,碱石灰增重的质量为二氧化碳和水的质量,则碱石灰增重的质量为:44g/mol×0.6mol+18g/mol×0.7mol=39g,
故答案为:39 g;
(3)反应②F与H发生酯化反应生成I:(CH3)3CCH2COOCH2CH2C(CH3)3,该反应也属于取代反应;反应③为醇的消去反应,
故答案为:取代反应;消去反应;
(4)D为(CH3)3CCH2ClCH3)、E为(CH3)3CCH=CH2,D→E为卤代烃的消去反应,其反应的化学方程式为:(CH3)3CCHClCH3+NaOH
| NaOH |
| △ |
故答案为:(CH3)3CCHClCH3+NaOH
| NaOH |
| △ |
(5)H为(CH3)3CCH2COOH,H的同分异构体中符合下列条件:①属于酯类化合物,分子中含有官能团酯基;②水解产物含有相同数目的碳原子,生成该酯的醇和羧酸具有相同的C原子,满足条件的酯有:CH3CH2COOCH2CH2CH3、CH3CH2COOCH(CH3)CH3,总共有两种,
故答案为:2.
点评:本题考查有机推断,为高考中的常见题型,属于中等难度的试题,试题贴近高考,综合性强,涉及烷、卤代烃、醇、醛、羧等,试题在注重对学生基础知识巩固与训练的同时,侧重对学生能力的培养与解题方法的指导和训练.该类试题能较全面地考查学生的有机化学基础知识和逻辑思维能力、创造思维能力,提高学生的应试能力和答题效率,也有利于培养学生的自学能力和知识的迁移能力.该题的关键是记住常见官能团的结构、性质以及官能团之间的相互转化,然后结合题意灵活运用即可.

练习册系列答案
相关题目
下列溶液一定呈中性的是( )
| A、pH=7的溶液 |
| B、c(H+)=c(OH-)=10-6mol/L溶液 |
| C、由强酸、强碱等物质的量反应后得到的溶液 |
| D、滴入甲基橙指示剂显橙色的溶液 |
能正确表示下列化学反应的离子方程式的是( )
| A、铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B、铝粉投入到NaOH溶液中:Al+2OH-═AlO2-+H2↑ |
| C、氯化铁溶液中加入铁粉:2Fe3++Fe═3Fe2+ |
| D、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
将15.6g Na2O2和5.4g Al同时放入一定量水中,充分反应后得到200ml澄清溶液,再向该溶液中缓慢通入HCl气体6.72L(标准状况),若反应中溶液体积不变,则下列判断正确的是( )
| A、反应过程中得到6.72L的气体(标准状况) |
| B、最终得到的溶液中c(Na+)=c(Cl-)+c(OH-) |
| C、最终得到7.8g沉淀 |
| D、最终得到的溶液中c(NaCl)=1.6mol/L |
 (其中R为烃基),相对分子质量为194.工业上以邻二甲苯(
(其中R为烃基),相对分子质量为194.工业上以邻二甲苯( )为原料先生产苯酐(
)为原料先生产苯酐( ),再使其与某醇在一定条件下反应可制得DMP.实验室由以下方法亦可得到DMP:
),再使其与某醇在一定条件下反应可制得DMP.实验室由以下方法亦可得到DMP: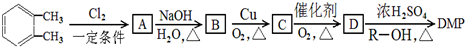
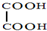 )在一定条件下可以按物质的量1:1发生反应可生成高分子化合物,反应的化学方程式为
)在一定条件下可以按物质的量1:1发生反应可生成高分子化合物,反应的化学方程式为
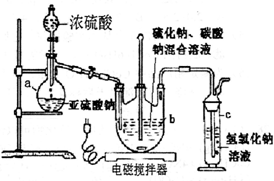 硫代硫酸钠(Na2S2O3?5H2O)俗名“大苏打”,又称为“海波”.它易溶于水,难溶于乙醇,加热易分解.工业上常用亚硫酸钠法、硫化碱法等制备.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图:实验具体操作步骤为:
硫代硫酸钠(Na2S2O3?5H2O)俗名“大苏打”,又称为“海波”.它易溶于水,难溶于乙醇,加热易分解.工业上常用亚硫酸钠法、硫化碱法等制备.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图:实验具体操作步骤为:
