题目内容
9.在水中加入下列物质,可使水的电离平衡正向移动的是( )| A. | NaCl | B. | Na2CO3 | C. | NH4Cl | D. | NaHSO4 |
分析 酸、强酸酸式盐或碱抑制水电离,含有弱离子的盐促进水电离,据此分析解答.
解答 解:A.NaCl是强酸强碱盐,不促进也不抑制水电离,故A错误;
B.碳酸钠是强碱弱酸盐,碳酸根离子水解促进水电离,水的电离平衡正向移动,故B正确;
C.氯化铵是强酸弱碱盐,铵根离子水解而促进水电离,水的电离平衡正向移动,故C正确;
D.硫酸氢钠在水溶液中完全电离,生成氢离子而使溶液呈强酸性,抑制水电离,水的电离平衡逆向移动,故D错误;
故选BC.
点评 本题以盐类水解为载体考查水的电离,为高频考点,明确酸、碱、盐影响水电离原理是解本题关键,易错选项是D,注意硫酸氢钠在水溶液中或熔融状态下电离方式区别,题目难度不大.

练习册系列答案
相关题目
19.下列有关化学用语表示正确的是( )
| A. | CH4分子的球棍模型: | B. | 聚氯乙烯的结构简式为CH2CHCl | ||
| C. | 3,3-二甲基-1-戊烯的键线式: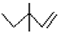 | D. | 乙醇分子的比例模型: |
20.有Na2CO3,Ba(OH)2,H2SO4三种体积和物质的量浓度都相等的溶液,几位同学按不同的顺序将它们混合(产生沉淀立即过滤掉),对于所得溶液,下列结论正确的是( )
| A. | 溶液一定显碱性 | B. | 溶液不可能显碱性 | ||
| C. | 溶液可能显碱性 | D. | 溶液不可能显酸性 |
14.下列叙述正确的是( )


| A. | A的结构简式是CH3CH2COOH | B. | B代表的是苯的结构模型 | ||
| C. | D代表的是甲烷 | D. | C和D互为同系物 |
18.下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:①N,⑥Si,⑦S,⑪Ca.
(2)在这些元素中,最活泼的金属元素是K(填元素符号,下同),最活泼的非金属元素是F.
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4(填写化学式,下同),碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3,写出这种两性氢氧化物与最强碱反应的化学方程式:Al(OH)3+KOH=KAlO2+2H2O;
(4)在③与④中,化学性质较活泼的是Na(填元素符号),怎样证明?(任写出一种实验事实即可)
Na与冷水剧烈反应,Mg与冷水发生缓慢反应.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 四 | ⑩ | ⑪ | ⑫ |
(2)在这些元素中,最活泼的金属元素是K(填元素符号,下同),最活泼的非金属元素是F.
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4(填写化学式,下同),碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3,写出这种两性氢氧化物与最强碱反应的化学方程式:Al(OH)3+KOH=KAlO2+2H2O;
(4)在③与④中,化学性质较活泼的是Na(填元素符号),怎样证明?(任写出一种实验事实即可)
Na与冷水剧烈反应,Mg与冷水发生缓慢反应.
16.将一小块钠投入下列溶液时,既能产生气体又会出现沉淀的是( )
| A. | 稀H2SO4 | B. | 氢氧化钠溶液 | C. | 硫酸铜溶液 | D. | 氯化钠溶液 |
