题目内容
已知HClO酸性是比H2CO3弱,反应Cl2+H2O?HCl+HClO达平衡后,要使HClO浓度增加可加入( )
| A、H2O |
| B、HCl |
| C、CaCO3 |
| D、NaOH(s) |
考点:弱电解质在水溶液中的电离平衡
专题:
分析:反应Cl2+H2O?HCl+HClO达平衡后,要使HClO浓度增大,可以采用加热、加入和盐酸反应的物质,据此分析解答.
解答:
解:A.加水稀释平衡向正反应方向移动,但次氯酸浓度降低,故A错误;
B.向溶液中通入HCl,盐酸浓度增大,平衡逆向移动,HClO浓度降低,故B错误;
C.向溶液中加入CaCO3,碳酸钙和稀盐酸反应导致平衡向正反应方向移动,次氯酸和碳酸钙不反应,所以次氯酸浓度增大,故C正确;
D.向溶液中加入NaOH,NaOH和HCl、HCl都反应,所以导致HClO浓度降低,故D错误.
故选:C.
B.向溶液中通入HCl,盐酸浓度增大,平衡逆向移动,HClO浓度降低,故B错误;
C.向溶液中加入CaCO3,碳酸钙和稀盐酸反应导致平衡向正反应方向移动,次氯酸和碳酸钙不反应,所以次氯酸浓度增大,故C正确;
D.向溶液中加入NaOH,NaOH和HCl、HCl都反应,所以导致HClO浓度降低,故D错误.
故选:C.
点评:本题考查了弱电解质的电离,根据物质性质确定平衡移动方向,从而确定次氯酸浓度变化,题目难度不大.

练习册系列答案
相关题目
能正确表示下列化学反应的离子方程式的是( )
| A、氢氧化钡溶液与盐酸的反应 OH-+H+=H2O |
| B、澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+=Ca2++2H2O |
| C、铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag |
| D、碳酸钙溶于稀盐酸中 CO32-+2H+=Ca2++H2O+CO2↑ |
莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是( )
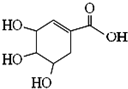

| A、分子式为C7H6O5 |
| B、分子中含有两种官能团 |
| C、可发生加成和取代反应 |
| D、分子中有7个碳原子共平面 |
将51.2g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.9mol,这些气体恰好能被500mL 2mol?L-1 NaOH溶液完全吸收,生成含NaNO3和NaNO2的盐溶液.下列说法不正确的是( )
| A、消耗硝酸的物质的量为2.5mol |
| B、气体中N2O4的物质的量为0.1mol |
| C、生成NaNO3的物质的量为0.2 mol |
| D、生成的氮的氧化物的混合气倒置于水槽中,通入标准状况下8.96L O2时,气体完全被吸收 |
将19.2g的铜溶于足量某浓度的硝酸溶液中,产生的气体(只含有NO、NO2)的标准状况下的体积为11.2L,则参加反应的硝酸的物质的量为( )
| A、0.6mol |
| B、0.8mol |
| C、1.2mol |
| D、1.1mol |
下列方法不能够生成Al(OH)3的是( )
| A、向AlCl3溶液中滴加Ba(OH)2溶液 |
| B、向NaAlO2溶液中滴加过量的HC |
| C、.向NaAlO2溶液中通入CO2 |
| D、l向AlCl3溶液中滴加氨水 |