题目内容
5.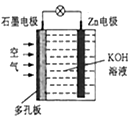 锌-空气电池(原理如图>适宜用作城市电动车的动力电源,放电时Zn转化为ZnO.则该电池放电时下列说法正确的是( )
锌-空气电池(原理如图>适宜用作城市电动车的动力电源,放电时Zn转化为ZnO.则该电池放电时下列说法正确的是( )| A. | 将电能转化为化学能 | B. | 氧气在石墨电极上发生还原反应 | ||
| C. | 电子由Zn电极经导线流向石墨电极 | D. | 该电池放电时OH-向石墨电极移动 |
分析 根据电池反应式知,锌作负极,负极上电极反应式为:Zn+2OH--2e-═ZnO+H2O,正极上通入空气,其电极反应式为O2+2H2O+4e-=4OH-,再结合离子移动方向分析解答.
解答 解:A.该装置为原电池装置,则将化学能转化为电能,故A错误;
B.氧气在正极,所以氧气在石墨电极上发生还原反应,故B正确;
C.电子由负极移向正极,所以电子由Zn电极经导线流向石墨电极,故C正确;
D.原电池工作时,溶液中的阴离子向负极移动,即OH-向Zn极移动,故D错误;
故选BC.
点评 本题考查了原电池原理,会根据电池反应式中元素化合价变化来确定正负极上发生的电极反应,注意电极反应式的书写与电解质溶液的酸碱性有关,难度不大,侧重于考查学生的分析能力和应用能力.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案
相关题目
15.根据表中7种短周期元素的有关信息判断,下列说法错误的是( )
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径/nm | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.152 |
| 最高化合价或最低化合价 | +1 | -2 | +3 | -1 | -2 | +3 | +1 |
| A. | 元素④气态氢化物的稳定性大于元素⑤气态氢化物的稳定性 | |
| B. | 元素②氢化物的沸点小于元素⑤氢化物的沸点 | |
| C. | 元素②⑥形成的化合物具有两性 | |
| D. | ⑦①可形成离子化合物 |
16.某电池总反应为2Fe 3++Cu=2Fe 2++Cu 2+,不能实现该反应的原电池是( )
| A. | 电极材料Fe、Cu,电解质溶液FeCl3溶液 | |
| B. | 电极材料石墨、Cu,电解质溶液Fe2(SO4)3溶液 | |
| C. | 电极材料Pt、Cu,电解质溶液FeCl3溶液 | |
| D. | 电极材料Ag、Cu,电解质溶液Fe2(SO4)3溶液 |
13.萜品醇可作为消毒剂、抗氧化剂和溶剂,已知α-萜品醇的结构简式如下式,则下列说法错误的是( )
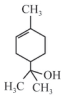

| A. | 1mol该物质最多能和1mol氢气发生加成反应 | |
| B. | 该物质不属于烃 | |
| C. | 该物质能使溴水褪色 | |
| D. | 分子式为C9H16O |
20.A、B、C、D四种物质均为下列离子组成的可溶性化合物,组成这四种物质的离子(离子不能重复组合)有:
分别取四种物质进行实验,实验结果如下:
①A、D溶液呈碱性,B呈酸性,C呈中性
②A溶液与B溶液反应生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失
③A溶液与D溶液混合并加热有气体生成,该气体能使湿润的红色石蕊试液变蓝
回答下列问题:
(1)A的化学式是Ba(OH)2.
(2)向A溶液中通入适量CO2,使A与CO2的物质的量之比为1:1.5,写出该反应的离子方程式:Ba2++4OH-+3CO2=BaCO3↓+HCO3-+H2O.
(3)写出③的离子方程式Ba2++2OH-+2NH4++CO32-$\frac{\underline{\;\;△\;\;}}{\;}$BaCO3↓+2NH3↑+2H2O.
| 阳离子 | Na+、Al3+、Ba2+、NH4+ |
| 阴离子 | Cl-、OH-、CO32-、SO42- |
①A、D溶液呈碱性,B呈酸性,C呈中性
②A溶液与B溶液反应生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失
③A溶液与D溶液混合并加热有气体生成,该气体能使湿润的红色石蕊试液变蓝
回答下列问题:
(1)A的化学式是Ba(OH)2.
(2)向A溶液中通入适量CO2,使A与CO2的物质的量之比为1:1.5,写出该反应的离子方程式:Ba2++4OH-+3CO2=BaCO3↓+HCO3-+H2O.
(3)写出③的离子方程式Ba2++2OH-+2NH4++CO32-$\frac{\underline{\;\;△\;\;}}{\;}$BaCO3↓+2NH3↑+2H2O.
1.下列说法不正确的是( )
| A. | CH3-CH=CH2和CH2=CH2的最简式相同 | |
| B. | 淀粉、纤维素都用(C6H10O5)n表示,二者互为同分异构体 | |
| C. | 下列物质的沸点按由低到高顺序为:(CH3)2CHCH3<(CH3)4C<(CH3)2CHCH2CH3<CH3(CH2)3CH3 | |
| D. | 等质量的甲烷、乙醇、乙醛分别充分燃烧,所耗用氧气的量依次减小 |
19.如图所示,其中甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O.下列说法不正确的是( )

| A. | 甲池通入CH3OH的电极反应为CH3OH-6e-+2H2O=CO32-+8H+ | |
| B. | 甲池中消耗280mL(标准状况下)O2,此时丙池中理论上最多产生1.45g固体 | |
| C. | 反应一段时间后,向乙池中加入一定量CuCO3固体,能使CuSO4溶液恢复原浓度 | |
| D. | 甲池是化学能转化为电能的装置,乙、丙池是电能转化为化学能的装置 |
 甲醇是一种优质燃料,可制作燃料电池.
甲醇是一种优质燃料,可制作燃料电池. 硫酸工业尾气中二氧化硫易造成环境污染,必须处理.用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法.其循环再生机理如图所示,
硫酸工业尾气中二氧化硫易造成环境污染,必须处理.用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法.其循环再生机理如图所示,