题目内容
16.某电池总反应为2Fe 3++Cu=2Fe 2++Cu 2+,不能实现该反应的原电池是( )| A. | 电极材料Fe、Cu,电解质溶液FeCl3溶液 | |
| B. | 电极材料石墨、Cu,电解质溶液Fe2(SO4)3溶液 | |
| C. | 电极材料Pt、Cu,电解质溶液FeCl3溶液 | |
| D. | 电极材料Ag、Cu,电解质溶液Fe2(SO4)3溶液 |
分析 电池总反应为 2Fe3++Cu═2Fe2++Cu2+,Cu失去电子,Fe3+得到电子,可知Cu为负极,正极为惰性电极或比Cu不活泼的金属,电解质溶液一定含铁离子,以此来解答.
解答 解:A.电极材料 Fe、Cu,电解质溶液 FeCl3 溶液,因Fe比Cu活泼,电池反应为2Fe3++Fe═3Fe2+,与题目不符,故A选;
B.电极材料石墨、Cu,电解质溶液 Fe2(SO4)3溶液,Cu作负极,电池总反应为 2Fe3++Cu═2Fe2++Cu2+,故B不选;
C.极材料 Pt、Cu,电解质溶液 FeCl3溶液,Cu作负极,电池总反应为 2Fe3++Cu═2Fe2++Cu2+,故C不选;
D.电极材料 Ag、Cu,电解质溶液 Fe2(SO4)3溶液,Cu作负极,电池总反应为 2Fe3++Cu═2Fe2++Cu2+,故D不选;
故选A.
点评 本题考查原电池的设计,把握电极判断、电池反应为解答的关键,侧重分析与应用能力的考查,注意Cu一定为负极且电解质为可溶性铁盐,题目难度不大.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
6.绿色化学的目标是( )
| A. | 减少对环境的污染 | |
| B. | 研究变换基本原料和起始化合物 | |
| C. | 设计对人类健康和环境更安全的化合物 | |
| D. | 防患于未然,最终杜绝化学污染源 |
7.物质的量的单位是( )
| A. | g | B. | L/mol | C. | mol | D. | g/mol |
4.在下列物质的溶液中滴入AgNO3溶液,产生淡黄色沉淀,加入稀HNO3后沉淀不消失的是( )
| A. | NaCl | B. | NaBr | C. | KI | D. | K2CO3 |
11.下列离子方程式中,正确的是( )
| A. | 小苏打溶液与少量澄清石灰水混合:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| B. | AlCl3溶液中加入足量的氨水:Al3++4OH-═AlO2-+2H2O | |
| C. | 碳酸氢铵溶液与足量的NaOH溶液共热,NH4++OH-?NH3↑+H2O | |
| D. | 向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
1.下列有关化学用语正确的是
( )
( )
| A. | NH4Br的电子式: | B. | 乙醇的分子式:C2H5OH | ||
| C. | 乙烯的结构简式为CH2CH2 | D. | CS2分子比例(填充)模型: |
8.下列指定反应的离子方程式正确的是( )
| A. | 锌粒与稀醋酸反应:Zn+2H+=Zn2++H2↑ | |
| B. | 碳酸镁跟硫酸反应:MgCO3+2H+=Mg2++H2O+CO2↑ | |
| C. | 氯化镁溶液与氨水反应:Mg2++2OH-=Mg(OH)2↓ | |
| D. | 氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
5.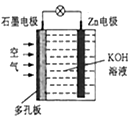 锌-空气电池(原理如图>适宜用作城市电动车的动力电源,放电时Zn转化为ZnO.则该电池放电时下列说法正确的是( )
锌-空气电池(原理如图>适宜用作城市电动车的动力电源,放电时Zn转化为ZnO.则该电池放电时下列说法正确的是( )
 锌-空气电池(原理如图>适宜用作城市电动车的动力电源,放电时Zn转化为ZnO.则该电池放电时下列说法正确的是( )
锌-空气电池(原理如图>适宜用作城市电动车的动力电源,放电时Zn转化为ZnO.则该电池放电时下列说法正确的是( )| A. | 将电能转化为化学能 | B. | 氧气在石墨电极上发生还原反应 | ||
| C. | 电子由Zn电极经导线流向石墨电极 | D. | 该电池放电时OH-向石墨电极移动 |
10.已知某元素R属于第四周期,它有6个价电子,其中只有1个价电子的电子云呈球形对称.则R的价电子排布式及所在的族是( )
| A. | 4s24p4;ⅢA | B. | 4p6;零族 | C. | 3d54s1;ⅥB | D. | 3d44s2;ⅥB |