题目内容
14. 某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A(g)+xB(g)?2C(g)达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如图所示.
某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A(g)+xB(g)?2C(g)达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如图所示.请回答下列问题:
(1)0~20min,A的平均反应速率为0.05;8min时,v(正)>v(逆).(填:“>”、“=”或“<”)
(2)反应方程式中的x=1,30min时改变的反应条件是降低了压强.
(3)20~30min时反应的平衡常数=30~40min时反应的平衡常数.(填:“>”、“=”或“<”).
分析 (1)0~20min内,A的浓度变化量为2mol/L-1mol/L=1mol/L,根据v=$\frac{△c}{△t}$计算v(A);
8min后,A的浓度继续减小,C的浓度继续增大,反应向正反应进行;
(2)由图象可知,30min时只有反应速率降低了,反应物与生成物的浓度瞬时降低,反应仍处于平衡状态,故不能是温度变化,而是降低了压强,故反应前后气体的体积不变,据此计算x的值;
(3)由(2)中分析可知,两阶段温度相同,温度相同,平衡常数相等.
解答 解:(1)0~20min内,A的浓度变化量为2mol/L-1mol/L=1mol/L,故v(A)=$\frac{1mol/L}{20min}$=0.05mol/(L•min);
8min后,A的浓度继续减小,C的浓度继续增大,反应向正反应进行,故v(正)>v(逆),
故答案为:0.05;>;
(2)由图象可知,30min时只有反应速率降低了,反应物与生成物的浓度瞬时降低,反应仍处于平衡状态,故不能是温度变化,而是降低了压强,故反应前后气体的体积不变,则x+1=2,故x=1,
故答案为:1;降低了压强;
(3)由(2)中分析可知,两阶段温度相同,温度相同,平衡常数相等,
故答案为:=.
点评 本题考查化学平衡图象问题,题目难度中等,本题注意根据图象浓度的变化以及影响化学反应速率的条件,本题易错,答题时注意思考.

练习册系列答案
相关题目
5.将相同质量的铜分别与过量浓硝酸、稀硝酸反应,下列叙述正确的是( )
| A. | 消耗硝酸的物质的量:前者少,后者多 | |
| B. | 反应中转移的电子总数:两者相同 | |
| C. | 反应速率:两者相同 | |
| D. | 反应生成气体的颜色:前者浅,后者深 |
19.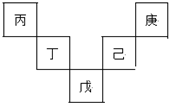 已知丙~庚元素在周期表(前四周期)中的相对位置如下图,其中己的最高氧化物对应水化物有强脱水性,丁原子最外层电子数是最内层电子数的2倍.下列判断错误的是( )
已知丙~庚元素在周期表(前四周期)中的相对位置如下图,其中己的最高氧化物对应水化物有强脱水性,丁原子最外层电子数是最内层电子数的2倍.下列判断错误的是( )
 已知丙~庚元素在周期表(前四周期)中的相对位置如下图,其中己的最高氧化物对应水化物有强脱水性,丁原子最外层电子数是最内层电子数的2倍.下列判断错误的是( )
已知丙~庚元素在周期表(前四周期)中的相对位置如下图,其中己的最高氧化物对应水化物有强脱水性,丁原子最外层电子数是最内层电子数的2倍.下列判断错误的是( )| A. | 丙与戊的原子序数相差28 | |
| B. | 常温下,庚的单质能与水反应产生气体 | |
| C. | 气态氢化物的稳定性:庚<己<戊 | |
| D. | 丁的最高价氧化物可用于制造光导纤维 |
6.将I2、Na2O、NaOH、Na2S、Na2SO4分别加热熔化,需要克服相同类型作用力的物质有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
4.某卤代烷烃C5H11Cl发生消去反应时,可以得到两种烯烃,则该卤代烷烃的结构简式可能为( )
| A. | CH3CH2CH2CH2Cl | B. | CH3CH2-CHCl-CH2CH3 | ||
| C. | CH3-CHCl-CH2CH2CH3 | D. | (CH3)3CCH2Cl |
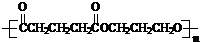 )是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下:
)是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下: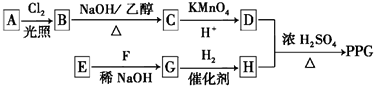
 .
.
 .
. .
. .
.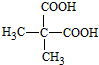 .
.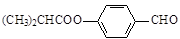 .合成M的一种途径如下:
.合成M的一种途径如下: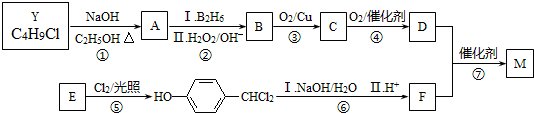
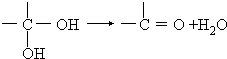
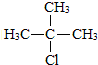 ,D的官能团名为羧基.
,D的官能团名为羧基.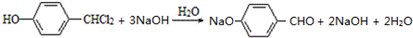 .
.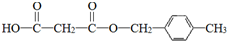 .
.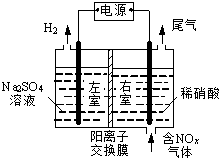 电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如右图所示(图中电极均为石墨电极).
电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如右图所示(图中电极均为石墨电极).