题目内容
7.写出下列各反应的化学方程式(是离子反应的只写出离子反程式)(1)铁和水蒸气的反应3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2
(2)铁和氧气(点燃)的反应3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4
(3)铝和盐酸的反应2Al+6H+=2Al3++3H2↑
(4)铝和氢氧化钠的反应2Al+2H2O+2OH-=2AlO2-+3H2↑.
分析 (1)铁和水蒸气在加热的条件下生成四氧化三铁和氢气;
(2)铁和氧气(点燃)发生化合反应生成四氧化三铁;
(3)铝与盐酸反应生成氯化铝和氢气;
(4)铝与NaOH溶液反应生成偏铝酸钠和氢气.
解答 解:(1)铁与水蒸气在加热条件下反应生成四氧化三铁和氢气,化学反应式为:3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2,
故答案为:3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2;
(2)铁和氧气(点燃)发生化合反应生成四氧化三铁,化学反应为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,
故答案为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(3)Al与盐酸反应生成氯化铝和氢气,反应为2Al+6HCl=2AlCl3+3H2↑,离子反应为2Al+6H+=2Al3++3H2↑,
故答案为:2Al+6H+=2Al3++3H2↑;
(4)铝与NaOH溶液反应生成偏铝酸钠和氢气,化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,离子反应为2Al+2H2O+2OH-=2AlO2-+3H2↑,
故答案为:2Al+2H2O+2OH-=2AlO2-+3H2↑.
点评 本题考查学生根据反应原理书写化学方程式的能力,侧重铁和铝的性质的考查,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等,注意掌握离子反应方程式的技巧,题目难度不大.

练习册系列答案
相关题目
17.下列说法不正确的是( )
| A. | 中和热测定实验中,应迅速将NaOH溶液和盐酸在测定装置中混合 | |
| B. | 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 | |
| C. | 探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mL H2O,向另一支试管中加入2mL 5%H2O2和1mL FeCl3溶液,观察并比较实验现象 | |
| D. | 已知4H++4I-+O2=2I2+2H2O,为了利用该反应探究反应速率与温度的关系,所用试剂除1 mol•L-1KI溶液、0.1 mol•L-1稀硫酸外,还需要用到淀粉溶液 |
18.下列反应中,离子方程式书写正确的是( )
| A. | 过量CO2与澄清石灰水反应:Ca2++2OH-+CO2═CaCO3↓+H2O | |
| B. | 向KHSO4溶液中加入Ba(OH)2溶液至所得溶液的pH=7 Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| C. | 向Ca(HCO3)2溶液中滴入过量的NaOH溶液Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O | |
| D. | 硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
15.下列说法正确的是( )
| A. | 将AgBr放入水中不能导电,故AgBr不是电解质 | |
| B. | CO2溶于水得到的溶液能导电,所以CO2是电解质 | |
| C. | 熔融的金属能导电,所以金属是电解质 | |
| D. | 固态的NaCl不导电,但 NaCl是电解质 |
2.一个原电池反应为:Fe+Cu2+═Fe2++Cu,该原电池的电极及电解质溶液可能是( )
| 正极 | 负极 | 电解质溶液 | |
| A | Fe | Cu | FeCl2溶液 |
| B | Cu | Fe | 稀H2SO4 |
| C | Cu | Fe | CuSO4溶液 |
| D | 石墨 | Fe | CuCl2溶液 |
| A. | A | B. | B | C. | C | D. | D |
19.某厂生产的BaCO3因含少量BaSO4而不纯,提纯的方法是;将产品加入足量的饱和Na2CO3溶液中,充分搅拌,过滤,若用100.0LNa2CO3溶液溶解1.0mol的BaSO4,则Na2CO3溶液的最初浓度不得低于[已知Ksp(BaSO4)=1.1×10-10;Ksp(BaCO3)=2.6×10-9]( )
| A. | 0.24mol•L-1 | B. | 0.25mol•L-1 | C. | 0.34mol•L-1 | D. | 0.35mol•L-1 |
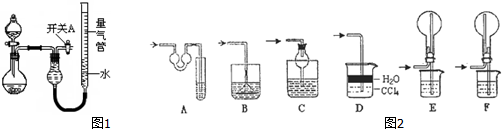
17.某同学设计如图1所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:
(1)实验过程中,使用分液漏斗滴加液体的操作是打开分液漏斗上口的活塞(或将活塞上的凹槽与瓶口上的小孔对齐),旋开分液漏斗的旋塞,缓慢滴加.
(2)该同学认为实验I可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?不可行(填“可行”或“不可行”).
(3)实验Ⅲ烧瓶中产生的SO2气体通入溴水溶液中发生反应的离子方程式是SO2+Br2+2H2O=4H++2Br-+SO42-.
(4)实验Ⅱ中量气管中的液体最好是c(填字母编号,下同).
a.浓NaOH溶液 b.氨水 c.煤油 d.氯化铵溶液
该实验剩余的NH3需吸收处理.图2各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有ACDF.
(5)本实验应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,②使量气管两端液面相平,③视线与凹液面最低处相平.
(6)实验Ⅳ获得以下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
根据上述数据,可计算出镁铝合金中铝的质量分数为27.0%.
| 实验 | 药品 | 制取气体 | 量气管中的液体 |
| Ⅰ | Cu、稀HNO3 | H2O | |
| Ⅱ | NaOH固体、浓氨水 | NH3 | |
| Ⅲ | Na2SO3固体、浓H2SO4 | SO2 | |
| Ⅳ | 镁铝合金、NaOH溶液(足量) | H2 | H2O |
(2)该同学认为实验I可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?不可行(填“可行”或“不可行”).
(3)实验Ⅲ烧瓶中产生的SO2气体通入溴水溶液中发生反应的离子方程式是SO2+Br2+2H2O=4H++2Br-+SO42-.
(4)实验Ⅱ中量气管中的液体最好是c(填字母编号,下同).
a.浓NaOH溶液 b.氨水 c.煤油 d.氯化铵溶液
该实验剩余的NH3需吸收处理.图2各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有ACDF.
(5)本实验应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,②使量气管两端液面相平,③视线与凹液面最低处相平.
(6)实验Ⅳ获得以下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
| 编号 | 镁铝合金度量 | 量气管第一次读数 | 量气管第二次读数 |
| ① | 1.0g | 10.0mL | 346.3mL |
| ② | 1.0g | 10.0mL | 335.0mL |
| ③ | 1.0g | 10.0mL | 345.7mL |