题目内容
已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
(1)用双线桥法分析上述反应(只需标出电子得失的方向和数目)
(2)上述反应中氧化剂是 ,氧化产物是 .硝酸没有全部参加氧化还原反应,没有参加氧化还原反应的硝酸占总硝酸的 .
(1)用双线桥法分析上述反应(只需标出电子得失的方向和数目)
(2)上述反应中氧化剂是
考点:氧化还原反应,氧化还原反应的电子转移数目计算
专题:氧化还原反应专题
分析:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O中,Cu元素的化合价由0升高为+2价,N元素的化合价由+5价降低为+2价,以此来解答.
解答:
解:(1)3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O中,Cu元素的化合价由0升高为+2价,N元素的化合价由+5价降低为+2价,该反应中转移6e-,电子得失的方向和数目为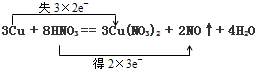 ,故答案为:
,故答案为: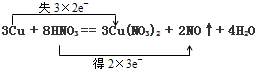 ;
;
(2)N元素的化合价降低,则HNO3为氧化剂,Cu元素失去电子被氧化,则Cu(NO3)2或Cu2+为氧化产物,由反应可知,8mol硝酸反应只有2mol硝酸作氧化剂,则没有参加氧化还原反应的硝酸占总硝酸的
=75%,故答案为:HNO3; Cu(NO3)2或Cu2+;75%.
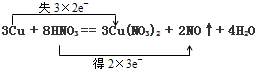 ,故答案为:
,故答案为: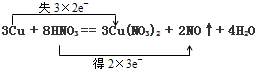 ;
;(2)N元素的化合价降低,则HNO3为氧化剂,Cu元素失去电子被氧化,则Cu(NO3)2或Cu2+为氧化产物,由反应可知,8mol硝酸反应只有2mol硝酸作氧化剂,则没有参加氧化还原反应的硝酸占总硝酸的
| 6 |
| 8 |
点评:本题考查氧化还原反应,为高频考点,侧重于学生的分析能力和应用能力的考查,明确反应中元素的化合价变化是解答的关键,题目难度不大.

练习册系列答案
相关题目
下列物质中不能用化合的方法制得的得( )
①SiO2 ②H2SiO3 ③Na2O2 ④FeCl2 ⑤FeCl3⑥CaSiO3.
①SiO2 ②H2SiO3 ③Na2O2 ④FeCl2 ⑤FeCl3⑥CaSiO3.
| A、①③⑤ | B、②④⑥ |
| C、② | D、②和④ |
把①蔗糖、②麦芽糖、③纤维素、④淀粉、⑤蛋白质在稀硫酸存在下分别进行水解,最终产物只有1种的是( )
| A、①和② | B、只有②③④ |
| C、只有③ | D、只有④ |
下列离子方程式正确的是( )
| A、向盐酸中滴加氨水:H++NH3?H2O=H2O+NH4+ |
| B、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| C、铜溶于稀硝酸:3Cu+8H++2NO3-=3Cu2++2 NO↑+4H2O |
| D、向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+ |