题目内容
下列实验操作中,正确的是( )
| A、为使过滤速率加快,可用玻璃棒在过滤器中轻轻搅拌,加速液体流动 |
| B、用酒精灯给试管加热时,要将被加热的试管放在酒精灯火焰的外焰上 |
| C、为加速固体物质的溶解只能采用加热的方法 |
| D、为增大气体物质的溶解度,常采取搅拌、加热等措施 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.过滤时应避免滤纸破损;
B.酒精灯外焰温度较高,可用外焰加热;
C.可用搅拌的方法加速溶解;
D.气体的溶解度随温度升高而降低.
B.酒精灯外焰温度较高,可用外焰加热;
C.可用搅拌的方法加速溶解;
D.气体的溶解度随温度升高而降低.
解答:
解:A.过滤时不能用玻璃棒搅拌,避免滤纸破损,故A错误;
B.酒精灯外焰温度较高,可用外焰加热,故B正确;
C.可用搅拌的方法加速溶解,加热不一定能促进溶解,如气体,故C错误;
D.气体的溶解度随温度升高而降低,加热不能增大溶解度,故D错误.
故选B.
B.酒精灯外焰温度较高,可用外焰加热,故B正确;
C.可用搅拌的方法加速溶解,加热不一定能促进溶解,如气体,故C错误;
D.气体的溶解度随温度升高而降低,加热不能增大溶解度,故D错误.
故选B.
点评:本题考查较为综合,涉及物质的分离、加热以及溶解等操作,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握操作的可行性的评价,难度不大.

练习册系列答案
相关题目
乙烯是重要的有机化工原料.下列关于乙烯的有关说法中不正确的是( )
| A、一种植物生长调节剂 |
| B、易燃 |
| C、能使溴水、酸性高锰酸钾溶液褪色 |
| D、与甲烷互为同系物 |
下列有关物质鉴别或检验的说法中,正确的是( )
| A、利用焰色反应鉴别NaHCO3和Na2CO3 |
| B、利用丁达尔效应鉴别淀粉胶体和氯化钠溶液 |
| C、滴入BaCl2溶液有白色沉淀,加入稀硝酸沉淀部分溶解,则原溶液中一定含SO42- |
| D、向溶液中先滴加氯水,再滴加KSCN溶液,溶液呈红色,说明原溶液中一定含Fe2+ |



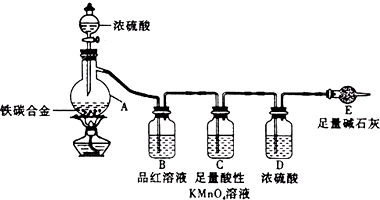 某校化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题.Ⅰ探究浓硫酸的某些性质
某校化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题.Ⅰ探究浓硫酸的某些性质