题目内容
下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
| A、将NaHCO3固体加入新制氯水中,有无色气泡(H+) |
| B、使红色布条退色(HCl) |
| C、向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈红色(Cl2) |
| D、滴加AgNO3溶液生成白色沉淀(Cl-) |
考点:探究氯水、氯气的漂白作用
专题:
分析:氯气与水反应,发生Cl2+H2O=H++Cl-+HClO,氯水中含有HClO、Cl2,具有氧化性,其中HClO具有漂白性,含有H+,具有酸性,以此解答.
解答:
解:A.氯水显酸性,能与碳酸氢钠反应生成CO2气体,故A不选;
B.次氯酸具有强氧化性,能氧化有色布条,故B选;
C.是氯气氧化了亚铁离子,故C不选;
D.氯离子和硝酸银反应生成氯化银白色沉淀,故D不选.
故选B.
B.次氯酸具有强氧化性,能氧化有色布条,故B选;
C.是氯气氧化了亚铁离子,故C不选;
D.氯离子和硝酸银反应生成氯化银白色沉淀,故D不选.
故选B.
点评:本题考查氯气的性质,侧重于氯水的组成和性质的考查,为高频考点,难度大不,注意把握相关物质的性质.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
某溶液中可能存在Mg2+、Fe2+、Fe3+,加入NaOH溶液,开始时是白色絮状沉淀,迅速变为灰绝色,最后变成红褐色.下列结论正确的是( )
| A、一定有Fe2+存在,一定没有Fe3+、Mg2+ |
| B、一定有Fe3+存在,一定没有Fe2+、Mg2+ |
| C、一定有Fe3+存在,可能有Fe2+,一定没有Mg2+ |
| D、一定有Fe2+ 存在,可能有Mg2+,一定没有Fe3+ |
常温下,下列各组物质不能用一种试剂通过化学反应区别的是( )
| A、MnO2 CuO FeO |
| B、(NH4)2SO4 K2SO4 NH4Cl |
| C、AgNO3 KNO3 Na2CO3 |
| D、Na2CO3 CaCO3 K2CO3 |
20℃时,11.6g由CO2和H2O组成的混合气体与足量的Na2O2充分反应,固体质量增加3.6g,则原混合气体的平均摩尔质量为(g/mol)( )
| A、5.8 | B、11.6 |
| C、23.2 | D、46.4 |
现在三组物质的分离:①含有水份的植物油中除去水份②回收碘的CCl4溶液中的CCl4③用食用酒精浸泡中草药提取其中的有效成分.分离以上各混合液的正确方法依次是( )
| A、分液、萃取、蒸馏 |
| B、萃取、蒸馏、分液 |
| C、分液、蒸馏、萃取 |
| D、蒸馏、萃取、分液 |
 某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.
某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.

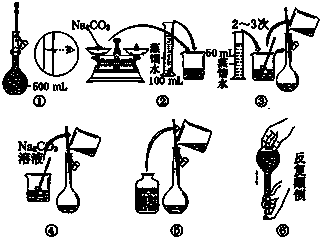 (1)若某药品质量约为32g
(1)若某药品质量约为32g