题目内容
某溶液中可能存在Mg2+、Fe2+、Fe3+,加入NaOH溶液,开始时是白色絮状沉淀,迅速变为灰绝色,最后变成红褐色.下列结论正确的是( )
| A、一定有Fe2+存在,一定没有Fe3+、Mg2+ |
| B、一定有Fe3+存在,一定没有Fe2+、Mg2+ |
| C、一定有Fe3+存在,可能有Fe2+,一定没有Mg2+ |
| D、一定有Fe2+ 存在,可能有Mg2+,一定没有Fe3+ |
考点:常见阳离子的检验
专题:物质检验鉴别题
分析:氢氧化钠与镁离子反应生成白色的氢氧化镁沉淀;与二价铁离子反应生成氢氧化亚铁,氢氧化亚铁不稳定能继续被空气氧化生成氢氧化铁,现象白色沉淀迅速变成灰绿色,最后变成红褐色;氢氧化钠与三价铁反应生成氢氧化铁红褐色沉淀,据此解答.
解答:
解:加入NaOH溶液,开始时有白色絮状沉淀,后迅速变为灰绿色,最后变为红褐色,该变化为亚铁离子与氢氧根离子反应的现象,据此判断一定存在亚铁离子,氢氧化铁为红褐色,颜色比白色深,若有铁离子存在,不会看到溶液中白色沉淀,所以一定不存在铁离子;镁离子与氢氧根离子反应生成白色的氢氧化镁沉淀,所以不能确定是否有镁离子,
故选:D.
故选:D.
点评:本题考查了常见离子的检验,题目难度中等,注意掌握常见离子的检验方法,熟记各种离子的特征反应,能够根据离子反应的特性正确推断离子种类.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、12g石墨烯(单层石墨)中含有六元环的个数为0.5NA |
| B、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为2NA |
| C、已知某种元素的一种原子的质量为 a g,则该元素的相对原子质量近似为a NA |
| D、78 g苯中含有C═C双键的数目为3NA |
下列说法正确的是:①明矾晶体是混合物②BaSO4是一种难溶于水的电解质③硫酸、纯碱、小苏打分别属于酸、碱、盐④氧化还原反应都属于离子反应⑤酸雨是指pH小于7.0的降水⑥丁达尔效应可以区分溶液和胶体.其中正确的是( )
| A、①②⑥ | B、①④⑤ |
| C、③④ | D、②⑥ |
下列离子检验的方法正确的是( )
| A、某溶液+AgNO3溶液→生成白色沉淀,说明原溶液中有Cl- |
| B、某溶液+BaCl2溶液→生成白色沉淀,说明原溶液中有SO42- |
| C、某溶液+NaOH溶液→生成蓝色沉淀,说明原溶液中有Cu2+ |
| D、某溶液+稀硫酸→产生无色气体,该气体能使澄清石灰水变浑浊,则原溶液中有CO32- |
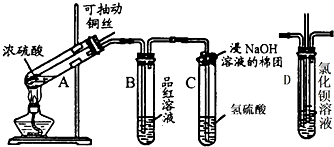
关于下图所示实验装置的叙述错误的是( )


| A、将水准管上提,液面高于量气管且不下降,说明装置不漏气 |
| B、若已知参加反应的Zn的质量,则该装置可用来测定气体摩尔体积 |
| C、若已知参加反应的Zn的质量,则该装置可用来测定锌的相对原子质量 |
| D、反应停止后,立即读数 |
下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
| A、将NaHCO3固体加入新制氯水中,有无色气泡(H+) |
| B、使红色布条退色(HCl) |
| C、向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈红色(Cl2) |
| D、滴加AgNO3溶液生成白色沉淀(Cl-) |