题目内容
5.铝的熔沸点比镁高的原因是( )| A. | 镁比铝活泼 | B. | 铝的化合价比镁高 | ||
| C. | 铝能与酸碱反应 | D. | 铝比镁的价电子多,半径比镁小 |
分析 根据金属原子半径越小,价电子数越多,则金属键越强,金属键越强其金属的硬度越大,熔沸点越高.
解答 解:铝的原子半径比镁小,价电子数比镁多一个,因此铝的金属键较强,硬度较大,所以铝的熔沸点比镁高,故D正确;
故选D.
点评 本题考查了金属键强弱的判定方法,难度不大,抓住金属原子半径越小,价电子数越多,则金属键越强是关键.

练习册系列答案
相关题目
15.下列对实验操作及结论的描述正确的是( )
| A. |  用于分离I2和NH4Cl | |
| B. |  用于测定某稀盐酸的物质的量浓度 | |
| C. | 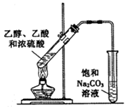 加热乙醇、乙酸和浓硫酸的混合液制取乙酸乙酯 | |
| D. |  滴入浓硫酸后,KMnO4溶液褪色,说明浓硫酸起到了脱水剂和氧化剂的作用 |
16.下列操作或记录的数据肯定正确的是( )
| A. | 用碱式滴定管量取16.00 mL KMnO4溶液 | |
| B. | 用乙醇萃取水溶液中的溴单质 | |
| C. | 用托盘天平称取5.6 g食盐 | |
| D. | 用标准盐酸滴定未知浓度的NaOH溶液消耗盐酸的体积为21.5 mL |
13.下列是一些同学在化学实验操作考试中的做法,你认为正确的是( )
| A. | 胶头滴管伸入量筒内滴加液体 | |
| B. | 用酒精灯的外焰给盛有液体(液体体积约占试管体积的$\frac{1}{4}$)的试管加热 | |
| C. | 称量完药品后,将药匙内剩余的药品放回试剂瓶 | |
| D. | 过滤时漏斗的末端在烧杯的中央 |
20.N2+3H2$?_{高温高压}^{催化剂}$2NH3制造氮肥的重要反应.下列关于该反应的说法正确的是( )
| A. | 增加N2的浓度能加快反应速率 | B. | 降低体系温度能加快反应速率 | ||
| C. | 使用催化剂不影响反应速率 | D. | N2足量时,H2能100%转化为NH3 |
10.下列单质中,最容易跟氢气发生反应,生成的氢化物最稳定的是( )
| A. | O2 | B. | N2 | C. | F2 | D. | Cl2 |
17.有机物X、Y分子式不同,它们只含C、H、O元素中的两种或三种,若将X、Y不论以何种比例混合,只要其物质的量之和不变,完全燃烧时耗氧气量和生成水的物质的量也不变.X、Y可能是( )
| A. | C2H6O和C2H4 | B. | C6H12O2和C5H12O | C. | C2H6O和C3H6O2 | D. | CH4和C2H4O2 |
14.各可逆反应达平衡后,改变反应条件,其变化趋势正确的是( )
| A. | 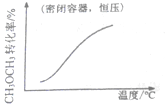 CH3OCH3(g)+3H2O(g)?6H2(g)+2CO2(g):△H>0 | B. | 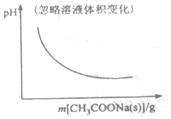 CH3COOH?H++CH3COO- | ||
| C. | 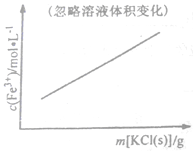 FeCl3+3KSCN?Fe(SCN)3+3KCl | D. | 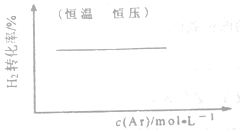 N2(g)+3H2(g)?2NH3(g) |
