题目内容
4.戊醇的同分异构体中与戊醇属于同类物质,且主链含四个碳原子的同分异构体有4种.分析 与戊醇属于同类物质,即属于醇类排除醚类,然后根据碳链异构和官能团位置异构写出同分异构体的结构简式,然后填空即可.
解答 解:根据碳链异构和官能团位置异构写出同分异构体:
CH3CH2CH(CH3)CH2OH 2-甲基-1-丁醇
(CH3)2 C(OH)CH2CH3 2-甲基-2-丁醇
(CH3)2 CHCH(OH)CH3 3-甲基-2-丁醇
(CH3)2 CHCH2CH2OH 3-甲基-1-丁醇,故总共有4种,
故答案为:4.
点评 本题主要考查的是醇的定义以及同分异构体的判断,难度不大,掌握醇类的碳链异构与官能团的位置异构是解决本题的关键.

练习册系列答案
相关题目
14.已知A,B、C,D、E是短期中原子序数依次增大的5种主族元素,其中元素A.E的单质在常温下呈气态.元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A. | 元素A、B组成的化合物常温下一定呈气态 | |
| B. | 一定条件下,元素C,D的最高氧化物对应的水化物之问能发生反应 | |
| C. | 工业上常用电解法制备元素A、C、D的单质 | |
| D. | 化合物AE与CE含有相同类型的化学键 |
15.单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点越高.下列溶液中沸点最高的是( )
| A. | 0.01 mol/L的蔗糖溶液 | B. | 0.02 mol/L的CH3COOH溶液 | ||
| C. | 0.02 mol/L的NaCl溶液 | D. | 0.01 mol/L的K2SO4溶液 |
12.下列关于化学与生产、生活的认识正确的是( )
| A. | 用米汤检验含碘盐中的碘酸钾 | |
| B. | 纤维素、蛋白质、塑料、天然橡胶都是高分子化合物 | |
| C. | 日常生活中常用无水乙醇进行杀菌消毒 | |
| D. | 光化学烟雾、臭氧层空洞、温室效应、硝酸型酸雨的形成都与氮氧化合物有关 |
9.高铁电池是一种新型可充电电池,电解液为KOH溶液,放电时的总反应式为:3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH下列叙述正确的是( )
| A. | 放电时,正极区溶液的pH减小 | |
| B. | 该电用电可用稀H2SO4代替KOH溶液 | |
| C. | 充电时,电解质溶液中的K+等阳离子向Zn电极移动 | |
| D. | 充电时,每转移3 mol电子,阳极有1 mol Fe(OH)3被还原 |
16.某小组以醋酸为例探究弱酸的性质.
(1)实验一:探究酸的强弱对酸与镁条反应速率的影响.
①设计实验方案如表,表中c=1.0 mol•L-1.
②实验步骤:a)检查装置(图1)的气密性后,添加药品;
b)反应开始后,每隔1min记录一次生成H2的体积;
c)将所记录的数据转化为曲线图(图2).
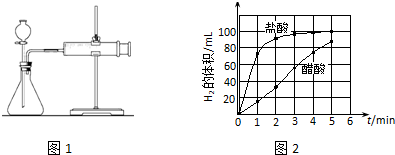
③写出0~5min醋酸、盐酸与镁条反应的反应速率变化规律:醋酸与镁条反应的速率随时间变化不明显,盐酸与镁条反应开始阶段反应速率很快,一段时间后反应速率明显减小.
(2)实验二:现有一瓶醋酸溶液,常温下测定其中醋酸的电离程度(已电离的电解质分子数占原来总分子数的百分比).
设计实验方案,将待测物理量和对应的测定方法填写在表中.
(1)实验一:探究酸的强弱对酸与镁条反应速率的影响.
①设计实验方案如表,表中c=1.0 mol•L-1.
| 编号 | 酸的种类 | 酸的浓度/mol•L-1 | 酸的体积/mL | 镁条质量/g |
| 1 | 醋酸 | 1.0 | 10 | 2.0 |
| 2 | 盐酸 | c | 10 | 2.0 |
b)反应开始后,每隔1min记录一次生成H2的体积;
c)将所记录的数据转化为曲线图(图2).

③写出0~5min醋酸、盐酸与镁条反应的反应速率变化规律:醋酸与镁条反应的速率随时间变化不明显,盐酸与镁条反应开始阶段反应速率很快,一段时间后反应速率明显减小.
(2)实验二:现有一瓶醋酸溶液,常温下测定其中醋酸的电离程度(已电离的电解质分子数占原来总分子数的百分比).
设计实验方案,将待测物理量和对应的测定方法填写在表中.
| 待测物理量 | 测定方法 |
| ①醋酸溶液的物质的量浓度 | 量取25.00ml醋酸溶液于锥形瓶中,滴加指示剂,将0.1000 mol•L-1 NaOH标准溶液装入 碱式滴定管,滴定至终点,记录数据.重复滴定2次. |
| ②H+的物质的量浓度 | 取适量醋酸溶液于烧杯中,用pH计测定溶液pH |
13.从海带中提取碘,可经过如图实验步骤完成.下列有关说法正确的是( )

| A. | 灼烧过程中使用的玻璃仪器有酒精灯、坩埚、玻璃棒 | |
| B. | 氧化过程中发生反应的离子方程式为:2I-+H2O2→I2+2OH- | |
| C. | 检验碘单质时,可选用淀粉碘化钾试纸,若试纸变蓝说明有碘单质 | |
| D. | 分液时,先打开活塞放出下层液体,再关闭活塞倒出上层液体 |
18.下列生产、生活中的事实不能用金属活动性顺序表解释的是( )
| A. | 铝制器皿不宜盛放酸性食物 | |
| B. | 电解饱和食盐水阴极产生氢气得不到钠 | |
| C. | 铁制容器盛放和运输浓硫酸 | |
| D. | 镀锌铁桶镀层破损后铁仍不易被腐蚀 |