题目内容
物质的量相等的CO和CO2相比较 ,下列有关叙述中正确的是
,下列有关叙述中正确的是
①它们所含的分子数目之比为1∶1
②它们所含的氧原子数目之比为1∶2
③它们所含的原子总数目之比为2∶3
④它们所含的碳原子数目之比为1∶1
A.①④ B.②③ C.①②④ D.①②③④
练习册系列答案
相关题目
硫代硫酸钠溶液与稀硫酸反应的化学方程式为Na2S2O3+H2SO4==Na2SO4+SO2↑+S↓+H2O,下列各组实验中最先出现浑浊的是( )
选 项 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | ||
A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
18.下列事实不能证明CH3COOH是弱电解质的是( )
| A. | 在CH3COONa溶液中通入SO2,生成CH3COOH | |
| B. | 等浓度的盐酸、CH3COOH溶液分别和锌反应,开始时盐酸的反应速率快 | |
| C. | 常温下0.1 mol•L-1 CH3COOH溶液的pH=2.1 | |
| D. | 用CH3COOH溶液做导电实验,灯泡很暗 |
19. 某学生用已知物质的量浓度的盐酸来滴定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生用已知物质的量浓度的盐酸来滴定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
(1)配制待测液,用5.0g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制1000mL溶液.除烧杯、量筒和胶头滴管外,还需要的玻璃仪器有1000ml容量瓶、玻璃棒.
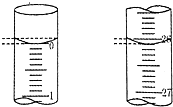
(2)滴定:用标准的盐酸溶液滴定待测的氢氧化钠溶液时,达到滴定终点的判断依据是:滴入最后一滴盐酸时,溶液由红色变为无色,并且半分钟之内不恢复红色,若滴定开始和结束时,酸式滴定管中的液面如图所示,则终点读数26.10mL.
(3)数据处理,某学生根据三次实验分别记录有关数据如下:
则该氢氧化钠溶液的物质的量浓度c(NaOH)=0.1044mol/L.(保留三位有效数字)
(4)若改用含Na2O杂质的NaOH配制成标准溶液来滴定盐酸,测得的盐酸浓度将偏低.(选填“偏高”、“偏低”或“无影响”)
 某学生用已知物质的量浓度的盐酸来滴定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生用已知物质的量浓度的盐酸来滴定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:(1)配制待测液,用5.0g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制1000mL溶液.除烧杯、量筒和胶头滴管外,还需要的玻璃仪器有1000ml容量瓶、玻璃棒.
(2)滴定:用标准的盐酸溶液滴定待测的氢氧化钠溶液时,达到滴定终点的判断依据是:滴入最后一滴盐酸时,溶液由红色变为无色,并且半分钟之内不恢复红色,若滴定开始和结束时,酸式滴定管中的液面如图所示,则终点读数26.10mL.
(3)数据处理,某学生根据三次实验分别记录有关数据如下:
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 0.00 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 |
| 第三次 | 25.00 | 0.22 | 26.31 |
(4)若改用含Na2O杂质的NaOH配制成标准溶液来滴定盐酸,测得的盐酸浓度将偏低.(选填“偏高”、“偏低”或“无影响”)


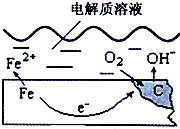 如图是钢铁在潮湿空气里发生电化学腐蚀原理示意图,发生的反应为:
如图是钢铁在潮湿空气里发生电化学腐蚀原理示意图,发生的反应为: