题目内容
1.实验室用63%的浓HNO3 (其密度为1.4g/mL)配制240mL 0.50mol/L稀HNO3,若实验仪器有:A.10mL量筒 B.50mL量筒 C.托盘天平 D.玻璃棒E.100mL容量瓶 F.250mL容量瓶 G.500mL容量瓶 H.胶头滴管 I.200mL烧杯.
(1)此浓硝酸的物质的量浓度为14.0mol/L
(2)应量取63%的浓硝酸8.9mL,应选用A.(填仪器的字母编号)
(3)实验时还需选用的仪器有(填序号) D、I、F、H
(4)配制过程中,下列操作会使配制的稀硝酸溶液浓度偏高的是(填序号)①③.
①量取浓硝酸的量筒用蒸馏水洗涤2-3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
(5)容量瓶是一种颈部细长的梨形瓶,由于其颈部细长,所以在向容量瓶中移入液体时,需要一定的耐心和技巧.有人建议将容量瓶的瓶颈改粗,对该建议的正确评价是B
A.可以按此建议改进,便于使用容量瓶
B.不能按此建议改进,因为会降低容量瓶的精确度
C.不必加粗瓶颈,因为向容量瓶中转移液体时,有少量液体倒出瓶外,不会对溶液的浓度产生太大影响.
分析 (1)根据物质的量浓度c=$\frac{1000ρω}{M}$来计算;
(2)设出需要的浓硝酸的体积,然后根据溶液稀释定律C浓V浓=C稀V稀来计算;根据“大而近”的原则,根据需要量取的浓硫酸的体积来选择合适的量筒;
(3)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
(4)根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
(5)容量瓶的瓶颈改粗,会降低容量瓶的精确度.
解答 解:(1)浓硫酸物质的量浓度c=$\frac{1000ρω}{M}$=$\frac{1000×1.4×63%}{63}$=14.0mol/L,
故答案为:14.0;
(2)由于无240mL容量瓶,故应选用250mL容量瓶,配制出250mL溶液,设需要的浓硝酸的体积为VmL,根据溶液稀释定律C浓V浓=C稀V稀:14.0mol/L×VmL=250mL×0.50mol/L,解得V=8.9mL;根据“大而近”的原则,根据需要量取的浓硝酸的体积为8.9mL,故应选择10mL量筒,
故答案为:8.9;A;
(3)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶可知所需的仪器有10mL量筒、烧杯、玻璃棒、250mL容量瓶和胶头滴管,故还需要的仪器有250mL容量瓶和胶头滴管,
故答案为:F、H;
(4)①量取浓硝酸的量筒用蒸馏水洗涤2-3次,并把洗涤液转入容量瓶,会导致溶质的量偏多,则浓度偏高,故①正确;
②容量瓶使用时未干燥,对浓度无影响,故②错误;
③溶解后未经冷却就移液,则冷却后溶液体积偏小,浓度偏高,故③正确;
④定容时不小心有少量蒸馏水滴到瓶外,会导致溶质的损失,则浓度偏低,故④错误;
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线是正常的,再加蒸馏水补至刻度线会导致浓度偏低,故⑤错误.
故答案为:①③;
(5)容量瓶的瓶颈改粗,会降低容量瓶的精确度,
故答案为:B.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,注意c=$\frac{n}{V}$理解应用,题目难度不大.

 名校课堂系列答案
名校课堂系列答案| A. | 盐酸 | B. | 醋酸 | C. | 硝酸 | D. | 硫酸 |
| A. | 都是强酸 | B. | 都是弱酸 | ||
| C. | a1 是强酸,a2 是弱酸 | D. | a1 是弱酸,a2 是强酸 |
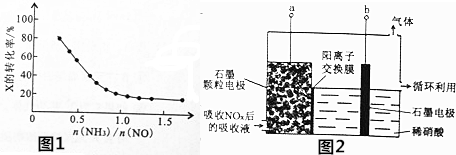
 ,下列有关叙述中正确的是
,下列有关叙述中正确的是