题目内容
8.存在于茶叶中的有机物A,其分子中所含的苯环上有2个取代基,取代基不含支链,且苯环上的一氯代物只有2种.A遇FeCl3溶液发生显色反应.F分子中除了2个苯环外,还有一个六元环.它们的转化关系如图: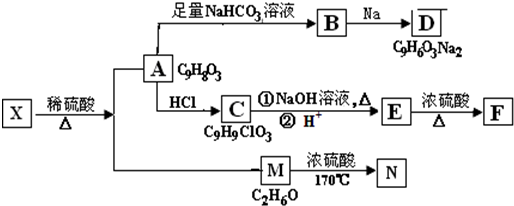
请回答下列问题:
(1)有机物A中含氧官能团的名称是酚羟基、羧基.
(2)E→F的反应类型是酯化反应.
(3)1mol A与Br2反应,最多可消耗Br2的物质的量是3 mol.
(4)写出A→B的化学方程式是
 +NaHCO3→
+NaHCO3→ +H2O+CO2↑.
+H2O+CO2↑.
分析 A的分子式为C9H8O3,分子中所含的苯环上有2个取代基,取代基不含支链,且苯环上的一氯代物只有2种,2个取代基处于对位,A遇FeCl3溶液发生显色反应,分子中含有酚羟基-OH,A能与碳酸氢钠反应,分子中含有羧基-COOH,A的不饱和度为$\frac{2×9+2-8}{2}$=6,故还含有C=C双键,所以A的结构简式为 ,X在浓硫酸、加热条件下生成A与M,M的分子式为C2H6O,M为乙醇,乙醇发生消去反应生成乙烯,N为乙烯,X为
,X在浓硫酸、加热条件下生成A与M,M的分子式为C2H6O,M为乙醇,乙醇发生消去反应生成乙烯,N为乙烯,X为 ,A与碳酸氢钠反应生成B,为
,A与碳酸氢钠反应生成B,为 ,B与Na反应生成D,D为
,B与Na反应生成D,D为 ,A与HCl反应生成C,C的分子式为C9H9ClO3,由A与C的分子式可知,发生加成反应,C再氢氧化钠水溶液中发生水解反应生成E,E在浓硫酸、加热的条件下生成F,F分子中除了2个苯环外,还有一个六元环,应发生酯化反应,故C为
,A与HCl反应生成C,C的分子式为C9H9ClO3,由A与C的分子式可知,发生加成反应,C再氢氧化钠水溶液中发生水解反应生成E,E在浓硫酸、加热的条件下生成F,F分子中除了2个苯环外,还有一个六元环,应发生酯化反应,故C为 ,E为
,E为 ,F为
,F为 ,据此解答.
,据此解答.
解答 解:A的分子式为C9H8O3,分子中所含的苯环上有2个取代基,取代基不含支链,且苯环上的一氯代物只有2种,2个取代基处于对位,A遇FeCl3溶液发生显色反应,分子中含有酚羟基-OH,A能与碳酸氢钠反应,分子中含有羧基-COOH,A的不饱和度为为$\frac{2×9+2-8}{2}$=6,故还含有C=C双键,所以A的结构简式为 ,
,
X在浓硫酸、加热条件下生成A与M,M的分子式为C2H6O,M为乙醇,乙醇发生消去反应生成乙烯,N为乙烯,X为 ,A与碳酸氢钠反应生成B,为
,A与碳酸氢钠反应生成B,为 ,B与Na反应生成D,D为
,B与Na反应生成D,D为 ,A与HCl反应生成C,C的分子式为C9H9ClO3,由A与C的分子式可知,发生加成反应,C再氢氧化钠水溶液中发生水解反应生成E,E在浓硫酸、加热的条件下生成F,F分子中除了2个苯环外,还有一个六元环,应发生酯化反应,故C为
,A与HCl反应生成C,C的分子式为C9H9ClO3,由A与C的分子式可知,发生加成反应,C再氢氧化钠水溶液中发生水解反应生成E,E在浓硫酸、加热的条件下生成F,F分子中除了2个苯环外,还有一个六元环,应发生酯化反应,故C为 ,E为
,E为 ,F为
,F为 ,
,
(1)由上述分析可知,有机物A为 ,分子中含氧官能团有:酚羟基和羧基,
,分子中含氧官能团有:酚羟基和羧基,
故答案为:酚羟基、羧基;
(2)E→F是 发生酯化反应生成
发生酯化反应生成 ,
,
故答案为:酯化反应;
(3) 与溴发生反应时,苯环羟基的邻位可以发生取代反应,C=C双键反应加成反应,故1molA可以和3mol Br2反应,
与溴发生反应时,苯环羟基的邻位可以发生取代反应,C=C双键反应加成反应,故1molA可以和3mol Br2反应,
故答案为:3;
(4)A→B的反应方程式为: +NaHCO3→
+NaHCO3→ +H2O+CO2↑,
+H2O+CO2↑,
故答案为: +NaHCO3→
+NaHCO3→ +H2O+CO2↑.
+H2O+CO2↑.
点评 本题考查有机物的推断,难度中等,是对有机物知识的综合考查,根据A的分子式及题目信息推断A的结构是解题的关键,能较好的考查学生分析、思维能力,是有机热点题型.

 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案| A. | 78 g过氧化钠晶体中,含2NA个阴离子 | |
| B. | 25℃时,1 L pH=12的Na2CO3溶液中含有Na+的数目为0.02NA | |
| C. | 常温常压下,28 g CO和N2的混合气体中含有的分子总数为NA | |
| D. | 标准状况下,22.4 L H2S和SO2的混合气体中含有的分子总数为NA |
| A. | 维生素C中氢的质量分数约为4.5% | |
| B. | 0.352g该试样中氧元素的质量为0.192g | |
| C. | 利用该实验所得数据计算可得维生素C的分子式为C3H4O3 | |
| D. | 维生素C是一种抗氧化剂,俗称抗坏血酸,它在中性或碱性溶液中易被氧化 |
| A. | Fe与盐酸反应 2Fe+6H+═2Fe3++3H2↑ | |
| B. | 碳酸钙与醋酸反应 CO32-+2CH3COOH═2CH3COO-+CO2↑+H2O | |
| C. | 氯气与H2O反应 Cl2+H2O═Cl-+2H++ClO- | |
| D. | 过量的CO2与Ca(ClO)2溶液反应:CO2+ClO-+H2O═HClO+HCO3- |
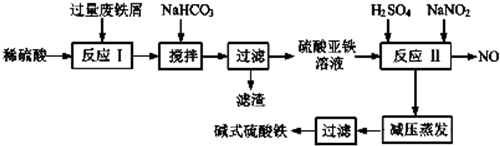
已知部分阳离子以氧氧化物形式沉淀时溶液的pH如下表.
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.0 | 4.4 |
(1)加入过量废铁屑的目的是使铁离子充分被还原为亚铁离子,同时防止亚铁离子被空气中氧气氧化(用离子方程式表示);加入少量NaHCO3的目的是Al3++3HCO3-=Al(OH)3↓+3CO2↑;该工艺中“搅拌”的作用是使反应物充分接触,加快反应速率,使反应充分进行;
(2)反应Ⅱ中的离子方程式为Fe2++2H++NO2-=Fe3++NO↑+H2O,该流程中可以循环、回收利用的物质是NO;
(3)生产碱式硫酸铁溶液蒸发时需要在减压条件下的原因是碱式硫酸铁受热易分解;
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-,为检测所得产品中是否含有Fe2+,应使用的试剂A.(填写字母)
| A.酸性KMnO4溶液 B.KSCN溶液 | C.氯水 D.NaOH溶液. |
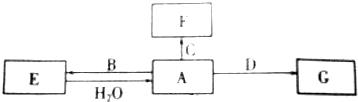
 ,写出E与H2O反应生成A的化学方程式2Na2O2+2H2O=4NaOH+O2↑
,写出E与H2O反应生成A的化学方程式2Na2O2+2H2O=4NaOH+O2↑