题目内容
2.在四个相同的容器中,分别进行合成氨的反应:N2(g)+3H2(g)?2NH3 (g),则反应速率最快的是( )| A. | v(NH3)=0.1 mol•L-1•min-1 | B. | v (H2)=0.6 mol•L-1•min-1 | ||
| C. | v (N2)=0.3 mol•L-1•min-1 | D. | v (H2)=0.3 mol•L-1•min-1 |
分析 根据化学反应速率之比等化学计量数之比进行计算,以同一个物质的化学反应速率进行比较,以此解答该题.
解答 解:N2(g)+3H2(g)?2NH3(g),可将各物质的反应速率转化为v(N2)进行比较,
A.v(N2)=$\frac{1}{2}$v(NH3)=0.05 mol•L-1•min-1;
B.v(N2)=$\frac{1}{3}$v (H2)=0.2 mol•L-1•min-1;
C.v (N2)=0.3 mol•L-1•min-1;
D.v(N2)=$\frac{1}{3}$v (H2)=0.1 mol•L-1•min-1,
则速率最大的为C.
故选C.
点评 本题考查化学反应速率的相关计算,为高频考点,侧重考查学生的分析能力,把握化学反应速率之比等化学计量数之比为解答的关键,难度不大.要注意比较化学反应速率快慢要以同一个物质进行比较.

练习册系列答案
相关题目
12.某元素基态原子的外围电子排布式为3d24s2,下列说法正确的是( )
| A. | 该元素位于元素周期表中第四周期ⅣB族 | |
| B. | 该元素位于s区 | |
| C. | 该元素的最高化合价为+2价 | |
| D. | 该元素基态原子中能量最高的是3d电子 |
13.聚对苯二甲酸乙二酯( 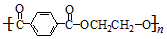 )简称PET,俗称“的确良”,是一种性能良好的树脂材料,常用于合成化学纤维.下列有关说法正确的是( )
)简称PET,俗称“的确良”,是一种性能良好的树脂材料,常用于合成化学纤维.下列有关说法正确的是( )
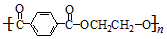 )简称PET,俗称“的确良”,是一种性能良好的树脂材料,常用于合成化学纤维.下列有关说法正确的是( )
)简称PET,俗称“的确良”,是一种性能良好的树脂材料,常用于合成化学纤维.下列有关说法正确的是( )| A. | 合成PET的单体为对苯二甲酸和乙醇 | |
| B. | PET可通过缩聚反应获得 | |
| C. | 1mol对苯二甲酸最多可以与5mol氢气发生加成反应 | |
| D. | PET与 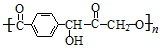 互为同分异构体 互为同分异构体 |
10.不粘锅内壁有聚四氟乙烯涂层,下列关于聚四氟乙烯的说法正确的是( )
| A. | 聚四氟乙烯的单体是不饱和烃 | |
| B. | 聚四氟乙烯中含有碳碳双键 | |
| C. | 聚四氟乙烯有固定熔点 | |
| D. | 四氟乙烯中既含有极性键又含有非极性键 |
17.对于X+Y(s)?Z的平衡体系,若增大压强,Y的平衡转化率增大,则X和Z可能的状态是( )
| A. | X为气态,Z为固态 | B. | X为固态,Z为气态 | C. | X为气态,Z为气态 | D. | X为固态,Z为固态 |
14.合成药物异搏定路线中某一步骤如图所示,下列说法正确的是( )


| A. | 物质X的分子式为C8H10O2 | |
| B. | 物质Y可以发生水解、加成和氧化反应 | |
| C. | 物质Z中所有原子有可能在同一平面内 | |
| D. | 物质X的同分异构体中含苯环且能水解的共有6种 |
 甲醇(CH3OH)燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源.
甲醇(CH3OH)燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源.