题目内容
11.已知,CO 的毒性表现在 CO 与血红蛋白(Hb)结合成 Hb•CO,使血红蛋白 失去输送 O2 功能.CO 进入血液后有如下平衡:CO+Hb•O2?O2+Hb•CO,已知在人 体体温 37℃下,该平衡常数为 220.试回答:(1)煤气中毒病人,可以通过进入高压氧舱的方法来救治,请用化学平衡的原理加以 说明:在高压氧舱中,煤气中毒患者吸入氧气浓度较高的空气后,CO+Hb•O2?O2+Hb•CO,平衡向左移,使Hb•CO转化为Hb•O2,恢复血红蛋白的输氧功能
(2)抽烟时,进入肺部的空气中 c(CO)=10-6mol/L,c(O )=10-2mol/L,则 c(Hb•CO)为 c(Hb•O2)的0.022倍.
(3)已知当血液中 c(Hb?CO)的比值大于 0.02 时,人的智力会很快受到损伤,为避免c(Hb?O2 )
人的智力受到损伤,c(O2)与 c(CO)的比值应大于11000.
分析 (1)在反应CO+Hb•O2?O2+Hb•CO中,增加氧浓度平衡逆向移动,减小CO与血红蛋白的结合,据此答题;
(2)根据$\frac{[{O}_{2}]•[Hb•CO]}{[CO]•[Hb•{O}_{2}]}$的比值进行计算;
(3)根据$\frac{[{O}_{2}]•[Hb•CO]}{[CO]•[Hb•{O}_{2}]}$的比值和 $\frac{[Hb•CO]}{[Hb•{O}_{2}]}$的比值计算.
解答 解:(1)在高压氧舱中,煤气中毒患者吸入氧气浓度较高的空气后,CO+Hb•O2?O2+Hb•CO,平衡向左移,使Hb•CO转化为Hb•O2,恢复血红蛋白的输氧功能,可以达到救治患者的目的,
故答案为:在高压氧舱中,煤气中毒患者吸入氧气浓度较高的空气后,CO+Hb•O2?O2+Hb•CO,平衡向左移,使Hb•CO转化为Hb•O2,恢复血红蛋白的输氧功能;
(2)因为c(CO)=10-6mol/L,c(O2)=10-2mol/L,根据$\frac{[{O}_{2}]•[Hb•CO]}{[CO]•[Hb•{O}_{2}]}$=220可知,$\frac{[Hb•CO]}{[Hb•{O}_{2}]}$=220×$\frac{1{0}^{-6}}{1{0}^{-2}}$=0.022,故答案为:0.022;
(3)$\frac{[{O}_{2}]•[Hb•CO]}{[CO]•[Hb•{O}_{2}]}$=220,$\frac{[Hb•CO]}{[Hb•{O}_{2}]}$>0.02,所以c(O2):c(CO)>$\frac{220}{0.02}$=11000,故答案为:11000.
点评 本题主要考查了反应方程式的书写及反应的条件、影响平衡移动的因素、及平衡常数的有关计算,中等难度,有一定的综合性.

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案| A. | 需用四个不同的量子数来描述原子中的每一个电子 | |
| B. | 在原子中,不能有两个电子具有一组相同的量子数 | |
| C. | 充满一个电子层需要8个电子 | |
| D. | 电子之间存在着斥力 |
| A. | v(NH3)=0.1 mol•L-1•min-1 | B. | v (H2)=0.6 mol•L-1•min-1 | ||
| C. | v (N2)=0.3 mol•L-1•min-1 | D. | v (H2)=0.3 mol•L-1•min-1 |
| A. | 1mol任何物质都含有约6.02×1023个原子 | |
| B. | 0.012kg12C约含有6.02×1023个碳原子 | |
| C. | 使用物质的量时,应用化学式指明粒子的种类 | |
| D. | 1mol H2的质量是1g |
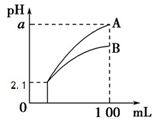 pH=2.1 的两种酸溶液 A、B 各 1mL,分别加水稀释到 100mL,其 pH 与溶液体积的关系如图,下列说法不正确的是( )
pH=2.1 的两种酸溶液 A、B 各 1mL,分别加水稀释到 100mL,其 pH 与溶液体积的关系如图,下列说法不正确的是( )| A. | 若 a<4.1,则 A、B都是弱酸 | |
| B. | 稀释后,A 酸溶液的酸性比B酸溶液强 | |
| C. | 若 a=4.1,则 A 是强酸,B是弱酸 | |
| D. | A、B两种酸溶液的物质的量浓度一定相等 |
| A. | 用稀硫酸洗掉铜器表面的铜锈 | |
| B. | 用混有少量Fe粉的Cu粉中,加入足量稀盐酸,充分反应后过滤 | |
| C. | 将KCl和MnO2(不溶于水)的混合物,加入足量水溶解,过滤 | |
| D. | 将混有少量CuCl2的FeCl2晶体,加入足量水溶解,过滤 |
| A. | 标准状况下,2.24 LCCl4中含Cl原子数目为0.4NA | |
| B. | 0.1mol苯乙烯中含有双键的数目为0.4NA | |
| C. | 14g聚乙烯中所含原子数为3NA | |
| D. | 常温常压下,10 g 46%酒精水溶液中含氧原子总数为0.1NA |
| A. | 标线 | B. | 温度 | C. | 浓度 | D. | 容量 |