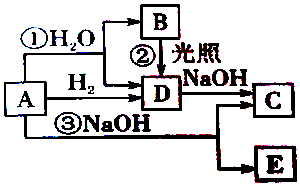
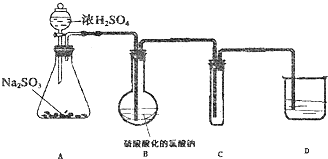
题目内容
6.在N2(g)+3H2(g)?2NH3(g);△H<0的反应中,下列叙述不正确的是( )(1)加压,使正反应速率加快,逆反应速率减慢;平衡向正反应方向移动
(2)升高温度,使正反应速率变慢、逆反应速率加快,平衡向逆反应方向移动
(3)使用催化剂,既加快正、逆反应速率,又有利于平衡向正反应方向移动
(4)温度越低,单位时向内氨的产量越高
(5)增大反应物浓度,平衡向正反应方向移动,反应物的利用率一定提高.
| A. | 只有(1)(2) | B. | 只有(1)(2)(3) | C. | 只有(4)(5) | D. | 全不正确 |
分析 该反应为可逆反应,反应物的转化率不可能达到100%,结合浓度、温度、催化剂对反应速率的影响解答该题.
解答 解:(1)加压,正逆反应速率都增大,故错误;
(2)升高温度,正逆反应速率都增大,故错误;
(3)使用催化剂,平衡不移动,故错误;
(4)温度越低,反应速率越小,单位时向内氨的产量越低,故错误;
(5)如加入反应物,增大反应物浓度,平衡向正反应方向移动,反应物的利用率降低,故错误.
故选D.
点评 本题考查化学反应速率的影响,为高考常见题型和高频考点,侧重于学生的分析能力和基本理论知识的综合理解和运用的考查,注意把握外界条件下对平衡移动和反应速率的影响,难度不大.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
16.等体积的硫酸铝、硫酸锌、硫酸钠溶液分别与足量氯化钡溶液反应.若生成硫酸钡沉淀的质量比为1:3:2,则三种硫酸盐的物质的量浓度之比为( )
| A. | 1:2:3 | B. | 1:4:9 | C. | 1:9:6 | D. | 1:6:3 |
17.现有以下仪器:烧杯、铁架台(带铁夹和铁圈)、酒精灯、玻璃棒、分液漏斗、蒸发皿、蒸馏烧瓶、导管、量筒、500mL容量瓶,根据这些仪器,下列实验可以进行的是( )
| A. | 制取蒸馏水 | B. | 配置500 mL 0.5 mol/L NaCl溶液 | ||
| C. | 除去CaCO3中混有的少量NaCl | D. | 分离食盐水和CCl4的混合液 |
11.与己二酸( )含有相同官能团的同分异构体有( )
)含有相同官能团的同分异构体有( )
 )含有相同官能团的同分异构体有( )
)含有相同官能团的同分异构体有( )| A. | 6 种 | B. | 7 种 | C. | 8 种 | D. | 9 种 |
15.将Mg、Al、Zn三种金属混合物与足量的稀硫酸反应,得3.36L氢气(标准状况),则三种金属的物质的量之和可能是( )
| A. | 0.125mol | B. | 0.15mol | C. | 0.2mol | D. | 0.215mol |
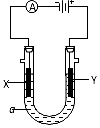 电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: