题目内容
1.观察实验:取3mL FeCl2溶液于试管中,用长滴管吸取3mL NaOH溶液,将长滴管尖嘴部分插入FeCl2溶液的底部后,快速挤出NaOH溶液,观察试管里的变化,现象:生成白色沉淀;离子方程式为Fe2++2OH-=Fe(OH)2↓.然后将上述溶液倒入表面皿,与空气充分接触,观察现象:白色絮状沉淀迅速变为灰绿色,最终变为红褐色,化学方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3,该反应类型为化合反应.氢氧化铁的形成:取少量FeC13溶液于试管中,滴入NaOH溶液,现象红褐色沉淀,离子方程式为Fe3++3OH-=Fe(OH)3↓.
得出结论:氢氧化亚铁与氢氧化铁的稳定性比较Fe(OH)3.
分析 氯化亚铁与氢氧化钠反应生成氢氧化亚铁,氢氧化亚铁不稳定,易被空气中氧气氧化,现象为白色絮状沉淀迅速变为灰绿色,最终变为红褐色,生成氢氧化铁,如制备氢氧化铁,可用氯化铁与氢氧化钠反应生成,氢氧化铁与氢氧化亚铁相比较,氢氧化铁较稳定,以此解答该题.
解答 解:取3mL FeCl2溶液于试管中,用长滴管吸取3mL NaOH溶液,将长滴管尖嘴部分插入FeCl2溶液的底部后,快速挤出NaOH溶液,观察试管里的变化,现象是生成白色沉淀;离子方程式为 Fe2++2OH-=Fe(OH)2↓.然后将上述溶液倒入表面皿,与空气充分接触,观察现象:白色絮状沉淀迅速变为灰绿色,最终变为红褐色,化学方程式 4Fe(OH)2+O2+2H2O=4Fe(OH)3,该反应类型为化合反应.
氢氧化铁的形成:取少量FeC13溶液于试管中,滴入NaOH溶液,现象生成红褐色沉淀,离子方程式为Fe3++3OH-=Fe(OH)3↓.
得出结论:氢氧化铁较稳定.
故答案为:生成白色沉淀;Fe2++2OH-=Fe(OH)2↓;白色絮状沉淀迅速变为灰绿色,最终变为红褐色;4Fe(OH)2+O2+2H2O=4Fe(OH)3;化合反应;红褐色沉淀;Fe3++3OH-=Fe(OH)3↓;Fe(OH)3.
点评 本题考查Fe的化学性质,为高频考点,把握物质的性质及发生的反应为解答的关键,侧重化学反应及现象的考查,注意现象与反应的对应关系,题目难度不大.

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
12.关于化学研究的意义,下列说法中正确的是( )
①保证人类的生存:诸如在解决人类粮食、能源、合理使用自然资源以及保护环境方面所作的努力和贡献;
②提高人类的生活质量:诸如合成新的材料,物质的净化和纯化等,均使人类衣、食、住、行的条件有大幅度的改善和提高;
③延长人类的寿命:诸如探明生命过程中的化学奥秘,合成新的药物等.
①保证人类的生存:诸如在解决人类粮食、能源、合理使用自然资源以及保护环境方面所作的努力和贡献;
②提高人类的生活质量:诸如合成新的材料,物质的净化和纯化等,均使人类衣、食、住、行的条件有大幅度的改善和提高;
③延长人类的寿命:诸如探明生命过程中的化学奥秘,合成新的药物等.
| A. | 只有①② | B. | 只有①③ | C. | 只有②③ | D. | ①②③ |
9.下列化学实验操作中,一般情况下不能相互接触的是( )
| A. | 用胶头滴管向试管滴液体时,滴管尖端与试管内壁 | |
| B. | 过滤操作中,漏斗颈与烧杯内壁 | |
| C. | 分液操作中,分液漏斗颈与烧杯内壁 | |
| D. | 过滤操作中,玻璃棒与三层滤纸 |
16.下列说法正确的是( )
| A. | 钢铁发生电化腐蚀的负极反应式:Fe-3e-═Fe3+ | |
| B. | 氢氧燃料电池的正极反应式:O2+2H2O+4e-═4OH- | |
| C. | 铜上镀锌时,与电源正极相连的是纯铜 | |
| D. | 用惰性电极电解饱和食盐水时,阴极的电极反应式为:2Cl--2e-═Cl2↑ |
6.在N2(g)+3H2(g)?2NH3(g);△H<0的反应中,下列叙述不正确的是( )
(1)加压,使正反应速率加快,逆反应速率减慢;平衡向正反应方向移动
(2)升高温度,使正反应速率变慢、逆反应速率加快,平衡向逆反应方向移动
(3)使用催化剂,既加快正、逆反应速率,又有利于平衡向正反应方向移动
(4)温度越低,单位时向内氨的产量越高
(5)增大反应物浓度,平衡向正反应方向移动,反应物的利用率一定提高.
(1)加压,使正反应速率加快,逆反应速率减慢;平衡向正反应方向移动
(2)升高温度,使正反应速率变慢、逆反应速率加快,平衡向逆反应方向移动
(3)使用催化剂,既加快正、逆反应速率,又有利于平衡向正反应方向移动
(4)温度越低,单位时向内氨的产量越高
(5)增大反应物浓度,平衡向正反应方向移动,反应物的利用率一定提高.
| A. | 只有(1)(2) | B. | 只有(1)(2)(3) | C. | 只有(4)(5) | D. | 全不正确 |
13.某烃的一种同分异构体只有一种一氯代物,则该烃的分子式可以是 ( )
| A. | C5H12 | B. | C6H14 | C. | C4H10 | D. | C7H16 |
10.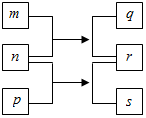 短周期元素W、X、Y、Z的原子序数依次增加.n、p、q是由这些元素组成的二元化合物,m是元素Y的单质,p是一种淡黄色粉末,q的水溶液可在玻璃器皿上蚀刻标记,0.01mol•L-1s溶液的pH为12,上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.n、p、q是由这些元素组成的二元化合物,m是元素Y的单质,p是一种淡黄色粉末,q的水溶液可在玻璃器皿上蚀刻标记,0.01mol•L-1s溶液的pH为12,上述物质的转化关系如图所示.下列说法正确的是( )
 短周期元素W、X、Y、Z的原子序数依次增加.n、p、q是由这些元素组成的二元化合物,m是元素Y的单质,p是一种淡黄色粉末,q的水溶液可在玻璃器皿上蚀刻标记,0.01mol•L-1s溶液的pH为12,上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.n、p、q是由这些元素组成的二元化合物,m是元素Y的单质,p是一种淡黄色粉末,q的水溶液可在玻璃器皿上蚀刻标记,0.01mol•L-1s溶液的pH为12,上述物质的转化关系如图所示.下列说法正确的是( )| A. | 离子半径:X>Y>Z | |
| B. | 氧化性:r>m | |
| C. | p和q中均含有离子键 | |
| D. | 等体积等浓度的q溶液与s溶液反应后,溶液呈中性 |
15.TiO2和TiCl4都是钛的重要化合物,某化学兴趣小组在实验室对两者的制备及性质进行探究.
Ⅰ.制备TiCl4
实验室利用反应TiO2 (s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,装置图和有关信息如下:
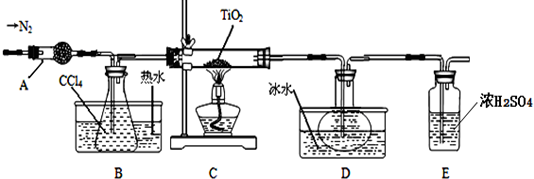
请回答下列问题:
(1)仪器A的名称是球形干燥管.
(2)实验开始前的操作包括:①组装仪器,②检验装置气密性,③加装药品,④通N2一段时间,⑤最后点燃酒精灯.实验结束后欲分离D中的液态混合物,所采用操作的名称是蒸馏(或分馏).
(3)装置E能否不能(填“能”或“不能”)换成装置A,理由是装置A不能吸收空气中的氧气,不能保证反应在无氧环境下进行.
Ⅱ.制备TiO2及测定TiO2的质量分数:
在TiCl4中加水、加热,水解得到沉淀TiO2•xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2.
(4)写出生成TiO2•xH2O的化学方程式TiCl4+(x+2)H2O$\frac{\underline{\;\;△\;\;}}{\;}$TiO2•xH2O↓+4HCl.
(5)一定条件下,将TiO2溶解并还原为Ti3+,用FeCl3标准溶液滴定Ti3+至全部生成Ti4+.滴定分析时,称取上述TiO2试样0.2g,消耗0.1mol•L-1 FeCl3标准溶液20mL.
①配制FeCl3标准溶液时,要加入一定量的盐酸,其目的是:抑制NH4Fe(SO4)2水解.
②该滴定操作所用到的指示剂是KSCN溶液.
③则TiO2质量分数为80%.
Ⅰ.制备TiCl4
实验室利用反应TiO2 (s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,装置图和有关信息如下:

| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
(1)仪器A的名称是球形干燥管.
(2)实验开始前的操作包括:①组装仪器,②检验装置气密性,③加装药品,④通N2一段时间,⑤最后点燃酒精灯.实验结束后欲分离D中的液态混合物,所采用操作的名称是蒸馏(或分馏).
(3)装置E能否不能(填“能”或“不能”)换成装置A,理由是装置A不能吸收空气中的氧气,不能保证反应在无氧环境下进行.
Ⅱ.制备TiO2及测定TiO2的质量分数:
在TiCl4中加水、加热,水解得到沉淀TiO2•xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2.
(4)写出生成TiO2•xH2O的化学方程式TiCl4+(x+2)H2O$\frac{\underline{\;\;△\;\;}}{\;}$TiO2•xH2O↓+4HCl.
(5)一定条件下,将TiO2溶解并还原为Ti3+,用FeCl3标准溶液滴定Ti3+至全部生成Ti4+.滴定分析时,称取上述TiO2试样0.2g,消耗0.1mol•L-1 FeCl3标准溶液20mL.
①配制FeCl3标准溶液时,要加入一定量的盐酸,其目的是:抑制NH4Fe(SO4)2水解.
②该滴定操作所用到的指示剂是KSCN溶液.
③则TiO2质量分数为80%.