题目内容
2.根据图转化关系以及实验现象填写空白.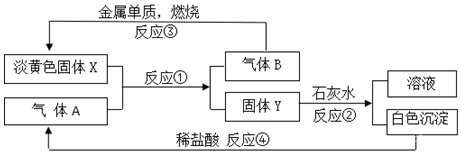
(1)气体A是CO2,图中溶液的溶质是NaOH(填写化学式).
(2)反应①的化学方程式是2Na2O2+2CO2=2Na2CO3+O2.
(3)反应④的离子方程式是CaCO3+2H+=Ca2++CO2↑+H2O.
分析 由图中转化可知,淡黄色固体X为Na2O2,B为O2,气体A为CO2,A与X反应生成B和Y,可知Y为Na2CO3,Na2CO3与石灰水反应生成白色沉淀为CaCO3,溶液为NaOH,以此来解答.
解答 解:(1)由上述分析可知A为CO2,溶液的溶质是NaOH,故答案为:CO2;NaOH;
(2)反应①的化学方程式是2Na2O2+2CO2=2Na2CO3+O2,故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(3)反应④的离子方程式是CaCO3+2H+=Ca2++CO2↑+H2O,故答案为:CaCO3+2H+=Ca2++CO2↑+H2O.
点评 本题考查无机物的推断,为高频考点,把握物质的性质、相互转化为解答关键,侧重分析与推断能力的考查,淡黄色为推断的突破口,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
9.下列关于水的说法中正确是( )
| A. | 在任何条件下,纯水都呈中性 | |
| B. | 在任何条件下,纯水的pH=7 | |
| C. | 在95℃时,纯水中 c(H+)<l0-7mol/L | |
| D. | 向纯水中加入少量 NaOH固体,水的电离逆向移动,c(OH-)降低 |
17.下列有关乙烯的说法中正确的是( )
| A. | 乙烯使溴水和酸性高锰酸钾溶液褪色原理相同 | |
| B. | 乙烯分子里所有原子都在同一个平面上,且碳氢键之间的键角约为 120° | |
| C. | 除去乙烷气体中的乙烯可以将混合气体通过盛有足量酸性高锰酸钾溶液的洗气瓶 | |
| D. | 乙烯和环丙烷(  )的分子组成符合通式 CnH2n,因此它们属于同系物 )的分子组成符合通式 CnH2n,因此它们属于同系物 |
7.下列说正确的是( )
| A. | 物质的量就是1摩尔物质的质量 | B. | 1 mol水中含有2 mol氢和1 mol氧 | ||
| C. | 1 molH2中含有6.02个氢分子 | D. | NH3的摩尔质量是17g•mol-1 |
14.在碘水中加入Na2SO3溶液,发现碘水褪色,这是由于发生了反应:Na2SO3+I2+H2O=Na2SO4+2HI,请据此分析:在含有Na2SO3、NaI、NaBr的混合液中通入一定量的氯气后,将溶液蒸干并充分灼烧,所得剩余固体的物质组成可能是( )
| A. | NaCl | B. | NaCl、NaBr、Na2SO4 | ||
| C. | NaCl、Na2SO4、I2 | D. | NaCl、NaI、Na2SO4 |
11.下列分子中属于含极性键的非极性分子的是( )
| A. | Cl2 | B. | CS2 | C. | CCl4 | D. | NH3 |
12.下列实验能成功的是( )
| A. | 用CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热 | |
| B. | 苯和浓溴水反应制溴苯 | |
| C. | CH3CH2Br中加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型 | |
| D. | 将乙酸和乙醇混合加热制乙酸乙酯 |
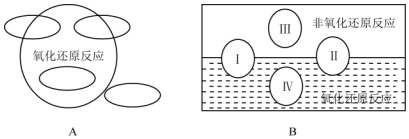 氧化还原是常见的反应类型,根据信息回答以下问题:
氧化还原是常见的反应类型,根据信息回答以下问题: