题目内容
下列物质在水溶液中的电离方程式书写正确的是( )
| A、HF═H++F- |
| B、Ba(OH)2═Ba2++2OH- |
| C、H3PO4═3H++PO43- |
| D、NH3?H2O═NH4++OH- |
考点:电离方程式的书写
专题:
分析:A.氢氟酸为弱酸,部分电离;
B.氢氧化钡为强电解质,完全电离,用“=”号,电荷守恒、离子符号正确次氯酸为弱酸,部分电离;
C.磷酸是中强酸,分步电离;
D.一水合氨是弱电解质,部分电离.
B.氢氧化钡为强电解质,完全电离,用“=”号,电荷守恒、离子符号正确次氯酸为弱酸,部分电离;
C.磷酸是中强酸,分步电离;
D.一水合氨是弱电解质,部分电离.
解答:
解;A.氢氟酸为弱酸,部分电离,用“?”号,其电离方程式为HF?H++F-,故A错误;
B.Ba(OH)2是强电解质,完全电离,用“=”号,电荷守恒、离子符号正确,电离方程式为Ba(OH)2═Ba2++2OH-,故B正确;
C.多元弱酸或多元中强酸分步电离,磷酸电离方程式为H3PO4═H++H2PO4-,故C错误;
D.弱电解质部分电离,用“?”号,NH3?H2O为弱碱,其电离方程式为:NH3?H2O?NH4++OH-,故D错误;
故选B.
B.Ba(OH)2是强电解质,完全电离,用“=”号,电荷守恒、离子符号正确,电离方程式为Ba(OH)2═Ba2++2OH-,故B正确;
C.多元弱酸或多元中强酸分步电离,磷酸电离方程式为H3PO4═H++H2PO4-,故C错误;
D.弱电解质部分电离,用“?”号,NH3?H2O为弱碱,其电离方程式为:NH3?H2O?NH4++OH-,故D错误;
故选B.
点评:本题主要考查电离方程式书写,掌握正确书写电离方程式的方法,并能正确判断电离方程式的正误是解答关键,注意多元弱酸分步电离,题目难度不大.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案
相关题目
下列事实不能用键能的大小来解释的是( )
| A、N元素的电负性较大,但N2的化学性质很稳定 |
| B、F2比O2更容易与H2反应 |
| C、HF、HCl、HBr、HI的稳定性逐渐减弱 |
| D、稀有气体一般难发生反应 |
特大洪水过后,受灾地区的水源常被严重污染,下列物质中能用于被污染的饮用水消毒杀菌的是( )
| A、生石灰 | B、漂白粉 |
| C、明矾 | D、硫酸铁 |
下列有关分散系的叙述正确的是( )
| A、Al(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的 |
| B、悬浊液中一定不含直径小于10-9m的微粒 |
| C、胶体区别于其他分散系的本质特征是胶体可发生丁达尔效应 |
| D、食盐溶液静置后会分层,下层比上层咸 |
三个容器中分别盛有H2、CH4、O2,已知三个容器中气体的温度、密度都相等,下列说法正确的是( )
| A、三种气体质量相等 |
| B、三种气体的物质的量之比为16:2:1 |
| C、三种气体压强比为16:2:1 |
| D、三种气体体积比为1:8:16 |
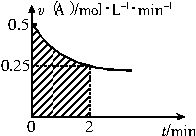 某溶液中发生反应A
某溶液中发生反应A| 无 |
| 无 |
| A、反应开始的前2min,A的平均反应速率小于0.375mol?L-1?min-1 |
| B、图中阴影部分的面积表示0~2min内A的物质的量浓度的减小值 |
| C、图中阴影部分的面积表示0~2min内A的物质的量的减小值 |
| D、至2min时,B的物质的量浓度c(B)介于1~1.5mol?L-1之间 |
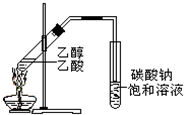 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: