题目内容
研究表明丰富的CO2完全可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)到本世纪中叶将枯竭的危机,同时又可缓解由CO2累积所产生的温室效应,实现CO2的良性循环
(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下转化生成甲醇蒸汽和水蒸气.如图表示恒压容器中0.5 mol CO2和1.5 mol H2转化率达80%时的能量变化示意图如图1.

写出该反应的热化学方程式 .
(2)工业上可用CO2与H2反应生成甲醇,在T℃下,将1molC O 2和2molH2充入5L恒容密闭容器中发生反应为CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得H2的物质的量随时间的变化情况如图2曲线I所示

①按曲线I计算反应从0到4min时,V(H2)=
②在T℃下,若仅改变的外界条件为 ,反应按曲线Ⅱ进行,计算达到平衡时容器中c(CO2)=
③判断该反应达到平衡的依据为 (填正确选项字母)
A混合气体的平均相对分子质量不随时间改变
B3v(H2)正=v(CH3OH)逆
C混合气体的压强不随时间改变
D单位时间内生成CH3OH和H2O的物质的量相同
(3)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸
①在不同温度下催化剂的催化效率与乙酸的生成速率如图所示,250~300℃时,温度升高而乙酸的生成速率降低的原因是
②将Cu2Al2O4溶解在稀硝酸的离子方程式为
(4)Li2O、Na2O、MgO均能吸收CO2
①如果寻找吸收CO2的其他物质,下列建议合理的是
a可在碱性氧化物中寻找
b可在ⅠA、ⅡA族元素形成的氧化物中寻找
c可在具有强氧化性的物质中寻找
②Li2O吸收CO2后,产物用于合成Li4SiO4用于吸收、释放CO2,原理是在500℃,CO2与Li4SiO4接触后生成Li2CO3,平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,说明该原理的化学方程式是 .
(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下转化生成甲醇蒸汽和水蒸气.如图表示恒压容器中0.5 mol CO2和1.5 mol H2转化率达80%时的能量变化示意图如图1.

写出该反应的热化学方程式
(2)工业上可用CO2与H2反应生成甲醇,在T℃下,将1molC O 2和2molH2充入5L恒容密闭容器中发生反应为CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得H2的物质的量随时间的变化情况如图2曲线I所示

①按曲线I计算反应从0到4min时,V(H2)=
②在T℃下,若仅改变的外界条件为
③判断该反应达到平衡的依据为
A混合气体的平均相对分子质量不随时间改变
B3v(H2)正=v(CH3OH)逆
C混合气体的压强不随时间改变
D单位时间内生成CH3OH和H2O的物质的量相同
(3)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸
①在不同温度下催化剂的催化效率与乙酸的生成速率如图所示,250~300℃时,温度升高而乙酸的生成速率降低的原因是
②将Cu2Al2O4溶解在稀硝酸的离子方程式为
(4)Li2O、Na2O、MgO均能吸收CO2
①如果寻找吸收CO2的其他物质,下列建议合理的是
a可在碱性氧化物中寻找
b可在ⅠA、ⅡA族元素形成的氧化物中寻找
c可在具有强氧化性的物质中寻找
②Li2O吸收CO2后,产物用于合成Li4SiO4用于吸收、释放CO2,原理是在500℃,CO2与Li4SiO4接触后生成Li2CO3,平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,说明该原理的化学方程式是
考点:热化学方程式,化学平衡的影响因素,化学平衡状态的判断
专题:
分析:(1)①根据图1可知0.5mol CO2和1.5mol H2转化率达80%时放热23-3.4=19.6KJ,然后按比例计算:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)的△H得出该反应的热化学方程式;
(2)①根据化学反应速率等于物质浓度的变化量和时间的比值来计算回答;
②根据到达平衡的时间减少,氢气也减少,说明改变了二氧化碳的浓度,先计算出曲线 I达到平衡时的平衡常数,根据温度不变,平衡常数不变再计算出曲线II达到平衡时CO2的浓度;
③依据反应平衡标志是正逆反应速率相同,各组分含量不变分析选项;
(3)(2)①根据温度对催化剂活性的影响;
②先将Cu2Al2O4拆成氧化物的形式:Cu2O?Al2O3,再根据氧化物与酸反应生成离子方程式,需要注意的是一价铜具有还原性;
(4)①二氧化碳为酸性气体,Li2O、Na2O、MgO均能吸收CO2与氧化性无关;
②在500℃,CO2与Li4SiO4接触后生成Li2CO3和另一种盐,该盐为Li2SiO3,据此书写反应原理方程式.
(2)①根据化学反应速率等于物质浓度的变化量和时间的比值来计算回答;
②根据到达平衡的时间减少,氢气也减少,说明改变了二氧化碳的浓度,先计算出曲线 I达到平衡时的平衡常数,根据温度不变,平衡常数不变再计算出曲线II达到平衡时CO2的浓度;
③依据反应平衡标志是正逆反应速率相同,各组分含量不变分析选项;
(3)(2)①根据温度对催化剂活性的影响;
②先将Cu2Al2O4拆成氧化物的形式:Cu2O?Al2O3,再根据氧化物与酸反应生成离子方程式,需要注意的是一价铜具有还原性;
(4)①二氧化碳为酸性气体,Li2O、Na2O、MgO均能吸收CO2与氧化性无关;
②在500℃,CO2与Li4SiO4接触后生成Li2CO3和另一种盐,该盐为Li2SiO3,据此书写反应原理方程式.
解答:
解:(1)①根据图1可知0.5mol CO2和1.5mol H2转化率达80%时放热23-3.4=19.6KJ,则该反应的热化学方程式:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-
×2=-49kJ?mol-1,
故答案为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49 kJ?mol-1;
(2)①V(H2)=
=0.05mol/(L?min),故答案为:0.05mol/(L?min);
②根据到达平衡的时间减少,氢气也减少,平衡正移,说明增大二氧化碳的浓度;
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始量(mol/L) 0.2 0.4 0 0
变化量(mol/L)
0.2
平衡量(mol/L)
0.2
平衡常数K=
Ⅱ图象中 设平衡时二氧化碳浓度为x
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始量(mol/L) 0.4 0 0
变化量(mol/L) 0.1 0.3 0.1 0.1
平衡量(mol/L) x 0.1 0.1 0.1
温度不变,平衡常数不变K=
=
,x=2.4mol/L
故答案为:增大二氧化碳的浓度;2.4mol/L;
③CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,反应是气体体积减小的放热反应;
A.反应前后气体质量不变,物质的量减小,混合气体的平均相对分子质量不随时间改变,说明反应达到平衡状态,故A正确;
B.v(H2)正=3v(CH3OH)逆,说明甲醇正逆反应速率相同,反应达到平衡,3v(H2)正=v(CH3OH)逆不能说明反应达到平衡状态,故B错误;
C.反应前后气体物质的量减小,混合气体的压强不随时间改变,说明反应达到平衡状态,故C正确;
D.单位时间内生成CH3OH和H2O的物质的量相同,说明反应正向进行,不能酸钠反应达到平衡状态,故D错误;
故答案为:AC;
(3)①温度超过250℃时,催化剂的催化效率降低,所以温度升高而乙酸的生成速率降低,故答案:温度超过250℃时,催化剂的催化效率降低;
②Cu2Al2O4拆成氧化物的形式:Cu2O?Al2O3,与酸反应生成离子方程式:3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O,
故答案为:3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O;
(4)①a.Li2O、Na2O、MgO均属于碱性氧化物,均能吸收酸性氧化物CO2,可在碱性氧化物中寻找吸收CO2的其他物质,故a正确;
b.Li2O、Na2O、MgO均能吸收CO2,钠、镁为ⅠA、ⅡA族元素,所以可在ⅠA、ⅡA族元素形成的氧化物中寻找吸收CO2的其他物质,故b正确;
c.Li2O、Na2O、MgO均能吸收CO2,但它们都没有强氧化性,且吸收二氧化碳与氧化还原无关,故c错误;
故答案为:ab;
②在500℃,CO2与Li4SiO4接触后生成Li2CO3,反应物为CO2与Li4SiO4,生成物有Li2CO3,根据质量守恒可知产物还有Li2SiO3,所以化学方程式为:CO2+Li4SiO4?Li2CO3+Li2SiO3,
故答案为:CO2+Li4SiO4?Li2CO3+Li2SiO3.
| 19.6 |
| 80% |
故答案为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49 kJ?mol-1;
(2)①V(H2)=
| ||
| 4min |
②根据到达平衡的时间减少,氢气也减少,平衡正移,说明增大二氧化碳的浓度;
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始量(mol/L) 0.2 0.4 0 0
变化量(mol/L)
| 0.2 |
| 3 |
| 0.2 |
| 3 |
| 0.2 |
| 3 |
平衡量(mol/L)
| 0.4 |
| 3 |
| 0.2 |
| 3 |
| 0.2 |
| 3 |
平衡常数K=
| 1 |
| 24 |
Ⅱ图象中 设平衡时二氧化碳浓度为x
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始量(mol/L) 0.4 0 0
变化量(mol/L) 0.1 0.3 0.1 0.1
平衡量(mol/L) x 0.1 0.1 0.1
温度不变,平衡常数不变K=
| 1 |
| 24 |
| 0.12 |
| 0.13x |
故答案为:增大二氧化碳的浓度;2.4mol/L;
③CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,反应是气体体积减小的放热反应;
A.反应前后气体质量不变,物质的量减小,混合气体的平均相对分子质量不随时间改变,说明反应达到平衡状态,故A正确;
B.v(H2)正=3v(CH3OH)逆,说明甲醇正逆反应速率相同,反应达到平衡,3v(H2)正=v(CH3OH)逆不能说明反应达到平衡状态,故B错误;
C.反应前后气体物质的量减小,混合气体的压强不随时间改变,说明反应达到平衡状态,故C正确;
D.单位时间内生成CH3OH和H2O的物质的量相同,说明反应正向进行,不能酸钠反应达到平衡状态,故D错误;
故答案为:AC;
(3)①温度超过250℃时,催化剂的催化效率降低,所以温度升高而乙酸的生成速率降低,故答案:温度超过250℃时,催化剂的催化效率降低;
②Cu2Al2O4拆成氧化物的形式:Cu2O?Al2O3,与酸反应生成离子方程式:3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O,
故答案为:3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O;
(4)①a.Li2O、Na2O、MgO均属于碱性氧化物,均能吸收酸性氧化物CO2,可在碱性氧化物中寻找吸收CO2的其他物质,故a正确;
b.Li2O、Na2O、MgO均能吸收CO2,钠、镁为ⅠA、ⅡA族元素,所以可在ⅠA、ⅡA族元素形成的氧化物中寻找吸收CO2的其他物质,故b正确;
c.Li2O、Na2O、MgO均能吸收CO2,但它们都没有强氧化性,且吸收二氧化碳与氧化还原无关,故c错误;
故答案为:ab;
②在500℃,CO2与Li4SiO4接触后生成Li2CO3,反应物为CO2与Li4SiO4,生成物有Li2CO3,根据质量守恒可知产物还有Li2SiO3,所以化学方程式为:CO2+Li4SiO4?Li2CO3+Li2SiO3,
故答案为:CO2+Li4SiO4?Li2CO3+Li2SiO3.
点评:本题考查了热化学方程式书写方法,化学反应速率、化学平衡状态影响因素分析应用,平衡计算的理解应用,平衡常数计算分析,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
形成原电池的条件一般有:①电解质溶液②两个电极③能自发地发生氧化还原反应④形成闭合回路
请根据上述条件判断下列装置中属于原电池的是( )
请根据上述条件判断下列装置中属于原电池的是( )
A、 NaCl溶液 |
B、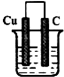 HCl溶液 |
C、 CuSO4溶液 |
D、 蔗糖溶液 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、标准状况下,2.24L苯中含C-H数目为0.6 NA |
| B、常温下,9.2gNO2和N2O4的混合气体中含有的氮原子数目为0.2NA |
| C、常温下,1.0LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA |
| D、在反应KClO3+6HCl═KCl+3Cl2↑+3H2O中,每生成3molCl2转移的电子数为6NA |
25℃时在五份蒸馏水中分别加入适量的下列物质,所得实验结果如下表表示:
加入物质后水的电离程度由大到小排列顺序正确的是( )
| 加入物质 | HCl(aq) | FeCl3 | NaOH | HCOONa | C2H5OH |
| 溶液的pH | 3 | 4 | 10 | 11 | 未测定 |
| 水的电离程度 | a1 | a2 | a3 | a4 | a5 |
| A、a3>a1>a5>a4>a2 |
| B、a4>a2>a5>a3>a1 |
| C、a2>a4>a5>a1>a3 |
| D、a1>a3>a5>a2>a4 |
下列离子方程式正确的是( )
| A、乙酸与碳酸钠溶液反应:2H++CO32-═CO2↑+H2O | ||
| B、醋酸溶液与新制氢氧化铜反应:CH3COOH+OH-═CH3COO-+H2O | ||
| C、苯酚钠溶液中通入少量二氧化碳:C6H5O-+CO2+H2OC6H5OH+CO32- | ||
D、甲醛溶液与足量的银氨溶液共热HCHO+4[Ag(NH3)2]++4OH-
|
除去下列物质中少量杂质的方法正确的是( )
| A、除去FeCl2溶液中混有的FeCl3:加足量铁粉,过滤 |
| B、除去Al2O3中混有的SiO2:加NaOH溶液,过滤 |
| C、除去CO2中混有的HCl:用饱和碳酸钠溶液洗气 |
| D、除去Cu粉中混有的CuO:加适量稀硝酸后,过滤 |
 近年来,我国部分地区多次陷入严重雾霾之中,其中一个重要的原因是我国的能源消费结构以燃煤为主,改变煤的利用方式可减少环境污染.以下是对煤进行处理的方法:
近年来,我国部分地区多次陷入严重雾霾之中,其中一个重要的原因是我国的能源消费结构以燃煤为主,改变煤的利用方式可减少环境污染.以下是对煤进行处理的方法: