题目内容
10.如图实验不合理的是( )| A. |  证明元素非金属性强弱 S>C>Si | B. |  四氯化碳萃取碘水中的碘 | ||
| C. |  制备并收集少量NO气体 | D. |  制备少量氧气 |
分析 A.发生强酸制取弱酸的反应;
B.碘不易溶于水,易溶于四氯化钛,且四氯化碳不溶于水;
C.Cu与稀硝酸反应生成NO,NO不溶于水;
D.过氧化钠为粉末状固体,关闭止水夹,不能使固液分离.
解答 解:A.发生强酸制取弱酸的反应可知酸性硫酸>碳酸>硅酸,则可比较非金属性S>C>Si,故A正确;
B.碘不易溶于水,易溶于四氯化钛,且四氯化碳不溶于水,则利于分液漏斗、四氯化碳可萃取碘水中的碘,故B正确;
C.Cu与稀硝酸反应生成NO,NO不溶于水,可利用排水法收集,则图中装置可制备并收集少量NO气体,故C正确;
D.过氧化钠为粉末状固体,关闭止水夹,不能使固液分离,则图中装置不能制备少量氧气,即不能控制反应的停止,故D错误;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、反应原理、实验装置的作用等为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合及实验评价性分析,题目难度不大.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
20.下列关于营养物质的说法正确的是( )
| A. | 蚕丝、羊毛、棉麻的主要成分都是蛋白质 | |
| B. | 淀粉、纤维素、油脂和蛋白质都属于天然高分子化合物 | |
| C. | 用甘氨酸和丙氨酸缩合最多可以形成4种二肽 | |
| D. | 蔗糖水解前后均可以发生银镜反应 |
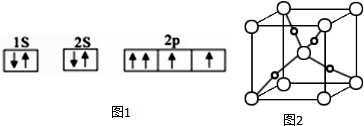
1.以下有关主族元素原子的“未成对电子”的说法,正确的是( )
| A. | 核外电子数为奇数的基态原子,其原子轨道中一定不含有“未成对电子” | |
| B. | 核外电子数为偶数的基态原子,其原子轨道中一定不含“未成对电子” | |
| C. | 核外电子数为偶数的基态原子,其原子轨道中可能含有“未成对电子” | |
| D. | 核外电子数为奇数的基态原子,其原子轨道中可能不含“未成对电子” |
18.某温度下,浓度都是1mol/L两种气体X2和Y2,在密闭容器中反应生成气体Z,经过t min后,测得物质的浓度为 (X2)=0.4mol/L,c(Y2)=0.8mol/L,c(Z)=0.4mol/L,则该反应的反应式可表示为( )
| A. | X2+2Y2=2Z | B. | 2X2+2Y2=2Z | C. | 3X2+Y2=2Z | D. | X2+3Y2=2Z |
15.制出了第一张元素周期表的化学家是( )
| A. | 门捷列夫 | B. | 阿伏伽德罗 | C. | 汤姆生 | D. | 道尔顿 |
19.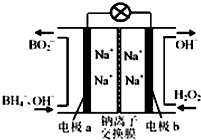 据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示,下列说法正确的是( )
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示,下列说法正确的是( )
 据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示,下列说法正确的是( )
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示,下列说法正确的是( )| A. | 电池放电时Na+从a极区移向b极区 | |
| B. | 电极a采用MnO2,放电时它被还原 | |
| C. | 该电池负极的电极反应式为:BH4-+8OH--8e-═BO2-+6H2O | |
| D. | 放电时,a极区的电极反应生成碱,碱性增强 |
20.设NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 常温下,100g46%乙醇水溶液中含有H原子数为12 NA | |
| B. | 23gNa与足量O2反应,生成Na2O 和Na2O2的混合物,转移的电子数为 NA | |
| C. | 标准状况下,2.24 LCCl4含有的共价键数为0.4 NA | |
| D. | 1 molN2与4molH2反应生成的NH3分子数小于2 NA |